Autor: Paul A. Webb
Dieser Artikel ist eine gekürzte Fassung eines umfassenderen Artikels mit dem Titel "Chemische Adsorption" als analytisches Verfahren.
Einführung
Katalysatoren werden in einer Vielzahl von Anwendungen eingesetzt, von der Herstellung von Konsumgütern bis hin zum Umweltschutz. Die optimale Gestaltung und effiziente Nutzung von Katalysatoren erfordert ein gründliches Verständnis der Oberflächenstruktur und der Oberflächenchemie des aktiven Materials. Chemische Adsorptionsverfahren ("Chemisorption") liefern einen Großteil der Informationen, die für die Bewertung von Katalysatormaterialien in der Entwurfs- und Produktionsphase sowie nach der Nutzungsdauer erforderlich sind. Obwohl ein Katalysator und die Reaktanten und Produkte in vielen Formen vorliegen können, befasst sich dieser Artikel mit den üblicherweise verwendeten heterogenen Katalysatoren.
Unterscheidung zwischen physikalischer und chemischer Adsorption
Ein charakteristisches Merkmal eines festen Materials ist die Verteilung von Stellen mit geringer Oberflächenenergie. Gas- oder Dampfmoleküle können an diese Stellen gebunden werden. Dies beschreibt im Allgemeinen das Phänomen der Adsorption. Die Menge der von der Oberfläche aufgenommenen Moleküle hängt von verschiedenen Bedingungen und Oberflächenmerkmalen ab, darunter die Temperatur, der Druck, die Verteilung der Oberflächenenergie und der Oberflächenbereich des Festkörpers. Ein Diagramm, das die Menge der adsorbierten Moleküle in Abhängigkeit vom Druck bei konstanter Temperatur darstellt, wird als Adsorptionsisotherme bezeichnet.
Physikalische Adsorption ("Physisorption") ist das Ergebnis relativ schwacher Van-der-Waal-Wechselwirkungskräfte zwischen der Festkörperoberfläche und dem Adsorbat - eine physikalische Anziehung. Physikalische Adsorption ist leicht umkehrbar.
Je nach Gas und Feststoff kann das Adsorptionsphänomen auch zum Austausch von Elektronen zwischen dem Adsorbat und der Festkörperoberfläche führen - eine chemische Bindung. Dies ist eine chemische Adsorption, die im Gegensatz zur Physisorption nur schwer wieder rückgängig gemacht werden kann. Um chemisch adsorbierte Moleküle zu entfernen, ist in der Regel eine beträchtliche Menge an Energie erforderlich.
Die physikalische Adsorption findet auf allen Oberflächen statt, sofern die Temperatur- und Druckbedingungen günstig sind. Chemisorption findet jedoch nur zwischen bestimmten Adsorbentien und adsorptiven Spezies statt und nur, wenn die Oberfläche von zuvor adsorbierten Molekülen gereinigt wurde.
Unter geeigneten Bedingungen kann die physikalische Adsorption dazu führen, dass die adsorbierten Moleküle mehrere Schichten bilden. Die Chemisorption hingegen verläuft nur so lange, wie das Adsorptionsmittel in direkten Kontakt mit der Oberfläche treten kann; sie wird in der Regel als einschichtiger Prozess betrachtet.
Ein Merkmal der physikalischen Adsorption ist, dass fast alle adsorbierten Moleküle bei derselben Temperatur, bei der die Adsorption stattfand, durch Evakuierung entfernt werden können. Die Erwärmung beschleunigt die Desorption, da sie den adsorbierten Molekülen die nötige Energie zur Verfügung stellt, um die Adsorptionsstelle zu verlassen.
Ein chemisch adsorbiertes Molekül ist stark an die Oberfläche gebunden und kann nicht ohne den Zufluss einer relativ großen Menge an Energie entweichen, verglichen mit der Energie, die erforderlich ist, um ein physikalisch gebundenes Molekül freizusetzen. Diese Energie wird durch Wärme bereitgestellt, und oft sind sehr hohe Temperaturen erforderlich, um eine Oberfläche von chemisch adsorbierten Molekülen zu reinigen.
Die Physisorption tritt in der Regel nur bei Temperaturen nahe oder unterhalb des Siedepunkts des Adsorptionsmittels bei dem herrschenden Druck auf. Dies ist bei der Chemisorption nicht der Fall. Die Chemisorption kann in der Regel bei Temperaturen weit oberhalb des Siedepunkts des Adsorptionsmittels stattfinden.
Die Beziehung zwischen Chemisorption und Katalyse
Ein Katalysator ist ein Material, das die Geschwindigkeit einer chemischen Reaktion beeinflusst. Ein Katalysator kann keine Reaktion auslösen, die sonst nicht stattfinden würde; er kann lediglich die Geschwindigkeit erhöhen, mit der sich die Reaktion dem Gleichgewicht nähert. Die Oberfläche eines "aktiven" Metalls besteht aus Chemisorptionsstellen. Trägerkatalysatoren sind solche, bei denen fein verteilte Körner des aktiven Metalls auf einem Trägermaterial abgeschieden sind. Die Körner, die sich auf der Oberfläche des Trägers befinden, stehen für die Reaktion mit dem Adsorptionsmittel zur Verfügung. Wenn die beschleunigte Reaktionsgeschwindigkeit einfach auf eine erhöhte Konzentration von Molekülen an der Oberfläche zurückzuführen wäre, könnte die Katalyse durch physikalische Adsorption der Reaktanten erfolgen. Dies ist nicht der Fall; die Chemisorption ist ein wesentlicher Schritt, der offensichtlich den Reaktanten (das adsorbierte Molekül) so verändert, dass er für eine chemische Reaktion empfänglicher wird. Die Abhängigkeit der Katalyse von der Bildung aktiver Zwischenverbindungen an der Oberfläche ist einer der Gründe, warum die Chemisorption als analytische Technik für die Untersuchung der Katalyse so wichtig ist.
Die Phasen eines heterogenen katalytischen Reaktionszyklus sind:
1) Diffusion (Transport) von Reaktanten an die Oberfläche des Katalysators
2) Chemisorption von Reaktanten
3) Oberflächenreaktionen zwischen chemisorbierten Spezies
4) Freisetzung von Produkten aus Katalysatoren
5) Diffusion von Produkten von der Oberfläche des Katalysators weg, um die Rückführung zu Schritt 1 zu ermöglichen
Die Vorhersage der Effizienz der Schritte 1 und 5 wird durch analytische Verfahren wie die physikalische Adsorption und die Quecksilberporosimetrie unterstützt, die die Porosität des Katalysatorbetts, des Katalysatormonolithen oder der einzelnen Körner des Katalysatormaterials charakterisieren. Die Charakterisierung der Schritte 2, 3 und 4 ist die Domäne der Chemisorptionsanalysen.
Chemisorptionstechniken und -methoden für die Bewertung von Katalysatoren
Chemisorptionsanalysen können zur Bestimmung der relativen Effizienz eines Katalysators bei der Förderung einer bestimmten Reaktion oder zur Untersuchung von Katalysatorvergiftungen und zur Überwachung der Verschlechterung der katalytischen Aktivität im Laufe der Nutzungsdauer eingesetzt werden.
Isotherme Chemisorptionsanalysen werden mit zwei Chemisorptionsverfahren durchgeführt: a) statische volumetrische Chemisorption und b) dynamische Chemisorption (strömendes Gas). Die volumetrische Technik eignet sich für eine hochauflösende Messung der Chemisorptionsisotherme von sehr niedrigem Druck bis zu atmosphärischem Druck bei praktisch jeder Temperatur von nahe der Umgebungstemperatur bis zu 1000 ºC oder mehr.
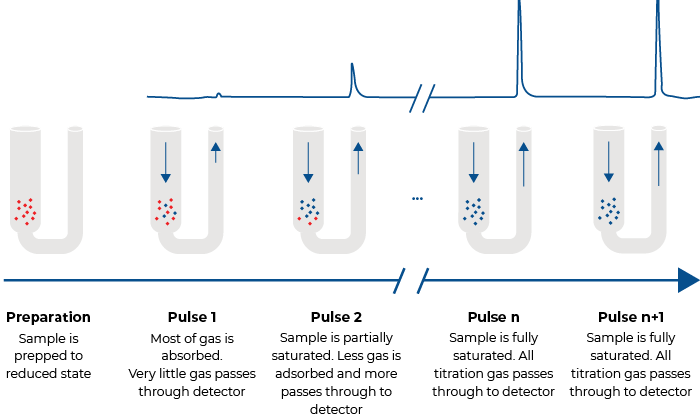
Die Impuls-Chemisorption, ein Strömungsgasverfahren, wird in der Regel bei Umgebungsdruck durchgeführt. Nachdem die Probe in einem Inertgasstrom gereinigt worden ist, werden kleine Mengen eines Reaktanten injiziert, bis die Probe gesättigt ist. Mit einem kalibrierten Wärmeleitfähigkeitsdetektor (TCD) wird bei jeder Injektion die Menge der von den aktiven Stellen aufgenommenen Reaktantenmoleküle bestimmt. Die ersten Injektionen können vollständig chemisorbiert sein; bei Sättigung wird keine der späteren Injektionen chemisorbiert sein, was auf Sättigung hindeutet. Die Anzahl der chemisorbierten Gasmoleküle steht in direktem Zusammenhang mit der aktiven Oberfläche des aktiven Materials.
Die Menge des chemisorbierten Gases pro Gramm Probe in Verbindung mit der Kenntnis der Stöchiometrie der Reaktion und der Menge des aktiven Metalls, das bei der Formulierung des Katalysators mit dem Trägermaterial vermischt wurde, ermöglicht die Berechnung der prozentualen Metalldispersion. Dies kann ein wichtiger Indikator für die Leistung des Katalysators und ein wichtiges wirtschaftliches Maß dafür sein, wie effizient das teure aktive Metall in einem Katalysatorprodukt eingesetzt wird.
Impuls-Chemisorption
Temperaturprogrammierte Desorption (TPD), temperaturprogrammierte Reduktion (TPR) und temperaturprogrammierte Oxidation (TPO) sind drei nicht-isotherme Methoden zur Charakterisierung von Katalysatoren. Bei der temperaturprogrammierten Desorption wird in der Regel kein Vakuum verwendet, so dass die Bedingungen in tatsächlichen industriellen Anwendungen besser simuliert werden. Bei der TPD-Analyse werden die Materialien in eine Probenzelle gegeben und zur Reinigung der aktiven Oberflächen vorbehandelt. Anschließend wird ein ausgewähltes Gas oder ein Dampf an die aktiven Stellen chemisorbiert, bis eine Sättigung erreicht ist. Danach werden die restlichen Moleküle mit einem Inertgas ausgespült.
Die Temperatur (Energie) wird mit kontrollierter Geschwindigkeit erhöht, während ein konstanter Inertgasstrom über der Probe aufrechterhalten wird. Das Inertgas und alle desorbierten Moleküle werden mit einem Wärmeleitfähigkeitsdetektor überwacht. Das TCD-Signal ist proportional zur Menge der desorbierten Moleküle, da die Wärmeenergie die Bindungsenergie überwindet. Die bei bestimmten Temperaturen desorbierten Mengen liefern Informationen über die Anzahl, Stärke und Heterogenität der Chemisorptionsstellen.
Temperaturprogrammierte Desorption (TPD)
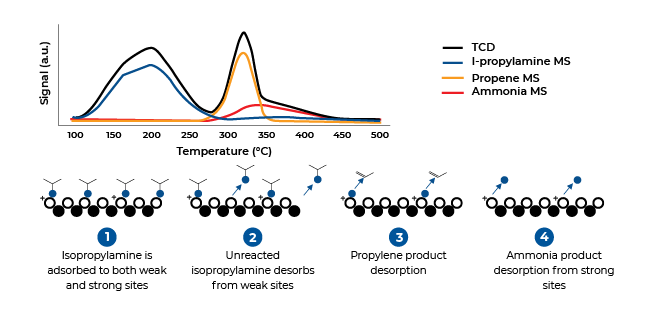
Programmierte Temperaturabsenkung (TPR)

Die temperaturprogrammierte Reduktion wird hauptsächlich zur Untersuchung der Reduzierbarkeit von Spezies wie Metalloxiden verwendet, die auf einem Träger dispergiert sind. Dabei wird ein Strom von verdünntem Wasserstoff (oder einem anderen Reduktionsmittel) über die Probe geleitet, während die Probentemperatur erhöht wird. Die Menge des verbrauchten Wasserstoffs und das Temperaturprofil, bei dem die Reduktion stattfand, werden gemessen. Ein Diagramm der verbrauchten Wasserstoffmenge im Verhältnis zur Temperatur kann einen oder mehrere Peaks ergeben, und die erhaltenen Daten geben Aufschluss über die Anzahl der reduzierbaren Spezies in der Probe sowie über deren Aktivierungsenergie.
Oberflächenenergie
Wenn eine feste Oberfläche einem Adsorptionsmittel ausgesetzt ist, werden die energiereichsten Stellen zuerst besetzt. Die Adsorptionswärme bei einem bestimmten Grad der Oberflächenbedeckung (Beladung) kann mit Hilfe der Clausius-Clapeyron-Gleichung berechnet werden. Dieser Ausdruck beschreibt die isosterische Adsorptionswärme in Abhängigkeit von Druck, Temperatur und der Gaskonstante und ist besonders auf Daten anwendbar, die mit volumetrischen Adsorptionsverfahren gewonnen wurden.
Die isosterische Adsorptionswärme über einen bestimmten Bereich kann anhand von Adsorptionsisothermen ermittelt werden, die den Druck im Verhältnis zur Temperatur bei einem konstanten adsorbierten Volumen darstellen. Die Isosteres werden aus einer Familie von Isothermen extrahiert, die für dasselbe Material bei verschiedenen Temperaturen ermittelt wurden. Die Steigung einer Isostere, aufgetragen auf einer logarithmischen Skala (lnP gegen 1/T)n, liefert einen Datenpunkt (qst, n), wobei n den mit der Isostere verbundenen Bedeckungsgrad darstellt. Eine Darstellung ähnlicher Punkte für verschiedene Bedeckungsgrade beschreibt die Verteilung der Oberflächenenergie als Funktion der Bedeckung. Diese Informationen helfen bei der Vorhersage der Aktivität eines Katalysators für eine bestimmte chemische Reaktion bei einer bestimmten Temperatur.
Die Aktivierungsenergie kann auch aus Daten abgeleitet werden, die mit der dynamischen Chemisorptionsmethode, insbesondere TPD, gewonnen wurden. Der Prozess bei dieser Methode verläuft in umgekehrter Richtung wie bei der statischen volumetrischen Technik. In diesem Fall wird Wärme (Energie) zugeführt, und mit steigender Temperatur werden Moleküle in der Reihenfolge der schwächsten Bindung freigesetzt. Die desorbierten Moleküle werden weggeschwemmt, und es findet keine Re-Sorption statt. Die Änderungsrate der Oberflächenbedeckung bzw. der Beladung ist mit der Änderungsrate der Temperatur verbunden.
Die Geschwindigkeit der einfachen molekularen Desorption kann mit Hilfe einer Kinetik 1. Ordnung modelliert werden, die üblicherweise als -kq ausgedrückt wird, wobei k die Geschwindigkeitskonstante ist, wobei das negative Vorzeichen eine Verringerung des Bedeckungsgrades mit der Zeit anzeigt und q den aktuellen Grad der Oberflächenbedeckung darstellt.
Die Geschwindigkeitskonstante k kann in der Arrhenius-Form ausgedrückt werden, A exp(-Ea/RT), wobei Ea die Aktivierungsenergie für die Desorption, T die absolute Temperatur und R die Gaskonstante ist. A ist bekannt als der vorexponentielle Faktor.
Die Kombination der oben dargestellten Beziehungen und Gleichungen führt letztendlich zu einem Ausdruck für die Aktivierungsenergie in Form von Variablen, die durch TPD-Analysen bestimmt werden können.
Zusammenfassung
Die Chemisorption ist ein grundlegender Prozess in der heterogenen Katalyse. Das Verständnis des Chemisorptionsprozesses im Zusammenhang mit einem Katalysator und einem Reaktanten ist der Schlüssel zur Kontrolle der Zusammensetzung und Herstellung von Katalysatoren und zur Bewertung von Katalysatoren. Analyseinstrumente, die chemische und physikalische Adsorptions- und Desorptionsisothermen messen können, sowie solche, die temperaturprogrammierte Reaktionen analysieren können, sind daher leistungsfähige Instrumente für die Untersuchung der Katalyse.