Einführung
Die Chemisorption ist eine leistungsstarke Analysemethode zur Untersuchung der Oberflächeneigenschaften fester Materialien, insbesondere von Katalysatoren. Im Gegensatz zur Physisorption, bei der schwache van-der-Waals-Wechselwirkungen auftreten, sind bei der Chemisorption starke Wechselwirkungen wie kovalente oder ionische Bindungen beteiligt. Diese Wechselwirkung ist sehr spezifisch, oft irreversibel und bildet nur eine Monolage. Die Wechselwirkung hängt stark von der chemischen Beschaffenheit sowohl der Oberfläche als auch des Adsorbats ab.
Chemisorptionsverfahren sind im Bereich der heterogenen Katalyse von wesentlicher Bedeutung, da Informationen wie Anzahl, Art und Stärke der aktiven Stellen auf einer Katalysatoroberfläche für die Optimierung der Leistung entscheidend sind. Solche Informationen ermöglichen es Wissenschaftlern, die Metalldispersion zu bestimmen und die Adsorptionsstärke, Aktivität und Reaktivität eines Katalysators zu bewerten, die die Schlüsselparameter bei der Entwicklung und Bewertung von Katalysatoren sind.
Zur Bewertung von Katalysatoren wurden bereits mehrere Chemisorptionsverfahren eingesetzt, darunter die Puls-Chemisorption und temperaturprogrammierte Analysen wie Reduktion, Oxidation, Desorption, Zersetzung und Oberflächenreaktionen. In dieser Application Note wird die Puls-Chemisorptionstechnik auf Micromeritics angewendet, um ihren Nutzen für die Katalysatorcharakterisierung mit dem ChemiSorb Auto zu demonstrieren.
Pulse Chemisorption Arbeitsprinzip
Bei der Pulse Chemisorption wird ein Strom von Wasserstoff in Argon in das Probenbett eingeleitet, um das aktive Metall bei erhöhter Temperatur zu reduzieren. Anschließend strömt ein Inertgas durch das Probenbett, um alle Rückstände des Reduktionsmittels bei erhöhter Temperatur zu entfernen. Die Probe wird auf Raumtemperatur abgekühlt. Abschließend wird je nach Art der aktiven Metalle eine bekannte Menge eines Prüfgases wie Wasserstoff (H2), Kohlenmonoxid (CO), Sauerstoff (O2) oder Distickstoffoxid (N2O) zudosiert.
Das System dosiert so lange, bis die Probe mit dem adsorbierten Gas gesättigt ist. Je nach Menge des adsorbierten Sondengases gelangt das nicht umgesetzte Gas zum Wärmeleitfähigkeitsdetektor (TCD) und erscheint als Peak im Detektorsignal. Die kalibrierte Schleife injiziert präzise eine bekannte Menge an Adsorbat in das Probenbett.
Auswahl des Adsorbats
Die Impulschemisorption ist eine weit verbreitete Technik zur Oberflächencharakterisierung, mit der die Anzahl der aktiven Stellen, die für chemische Reaktionen auf einem festen Material zur Verfügung stehen, quantifiziert werden kann (Metalldispersion). In einigen Anwendungen wird sie auch zur Untersuchung der aktiven Metalloberfläche eingesetzt. Die Auswahl eines geeigneten Adsorbats ist jedoch von entscheidender Bedeutung und sollte anhand von zwei Schlüsselfaktoren, dem stöchiometrischen Faktor und der Bindungsaffinität, sorgfältig geprüft werden.
Bei Metallen wie Kupfer und Silber ist die Bindungsaffinität fürH2 und CO vernachlässigbar, was zu einer geringen bis gar keiner Adsorption führt. Wenn jedoch N2Oals Adsorbat eingeführt wird, weist es eine starke Bindungsaffinität zu diesen Metallen auf, wodurch es sich besser für die Chemisorptionsanalyse eignet.
Sauerstoff wird üblicherweise bei der Puls-Chemisorption für die Wasserstoff-Sauerstoff-Titration verwendet. Im Falle von Palladium (Pd) neigt Wasserstoff dazu, mit dem Pd ein Hydrid zu bilden. Daher wird für Katalysatoren auf Pd-Basis oft CO bevorzugt. Die Verwendung von Wasserstoff kann jedoch auch problematisch sein, wenn der Katalysator auf einem Kohlenstoffträger sitzt, da der Träger selbst in erheblichem Maße Wasserstoff adsorbieren kann, was zu ungenauen Messungen führt.
Für Platin (Pt) können sowohl H2 als auch CO in Impuls-Chemisorptionsversuchen verwendet werden, da beide an der Metalloberfläche adsorbieren können. Die Wahl des Adsorbats wirkt sich jedoch auf den stöchiometrischen Faktor aus, der bei der Berechnung der Metalldispersion verwendet wird. Wasserstoff bindet dissoziativ an Pt, was zu einem stöchiometrischen Faktor von 2 führt, während CO entweder linear oder verbrückt binden kann, jeweils mit unterschiedlichen stöchiometrischen Faktoren. Für das Pt/Al2O3-Standardmaterial bindet CO linear, was einem stöchiometrischen Faktor von 1 entspricht.
Ergebnisse und Diskussion
Für diese Art der Analyse wurde 0,5 %iges Platin-Aluminiumoxid auf dem ChemiSorb Auto unter Verwendung vonH2 und CO als Prüfgas mit einer Metalldispersionsspezifikation von 31 % ± 5 % bewertet. Die Abbildungen 1A und 1B zeigen Puls-Chemisorptionsprofile unter Verwendung von 10 %H2/Ar bzw. 10 % CO/He als Prüfgas. Die Wärmeleitfähigkeiten vonH2 und Ar im Vergleich zu Luft betragen 7,07 bzw. 0,68. Dieser signifikante Unterschied ermöglicht es der TCD, das nicht umgesetzteH2-Signal effektiv zu unterscheiden.
In einigen Fällen, in denen eine 10%igeH2/Ar-Mischung nicht verfügbar ist, kann Stickstoff als alternatives Trägergas verwendet werden. Da die Wärmeleitfähigkeit von N2 im Vergleich zu Luft 1,00 beträgt, eignet sich ein 10%iges H2/N2-Gemisch auch für Puls-Chemisorptionsanwendungen.
Im ersten Versuch, bei dem 10 %H2/Ar als Adsorbat verwendet wurden (Abbildung 1A), wurde der erste Peak vollständig von der Probe verbraucht; ein ideales Szenario, das auf eine vollständige Adsorption hinweist. Der zweite Peak entsprach der Phase der teilweisen Sättigung, in der der größte Teil des Gases das Probenrohr verließ und das TCD erreichte. Die letzten drei Peaks zeigten an, dass die Probe mit Wasserstoffgas gesättigt war; daher waren weitere Injektionen unnötig.
Auch im zweiten Versuch, bei dem ein 10 %iges CO/He-Gemisch als Adsorbat verwendet wurde (Abbildung 1B), zeigte der erste Peak den vollständigen Verbrauch des Adsorbats durch das aktive Metall an. Der zweite und dritte Peak entsprachen einer teilweisen Sättigungsphase. Das Gerät hörte auf, Gas in das System einzuspritzen, sobald die Differenz zwischen aufeinanderfolgenden Peakflächen innerhalb von 5 % lag.
Durch Integration der Peakflächen und Berechnung der kumulativen Menge des adsorbierten Gases. So erhält man Informationen über die Metalldispersion, die metallische Oberfläche und die Kristallitgröße. Sechs Analysen dieser bestimmten Charge von Standardmaterial wurden mit demselben ChemiSorb Auto-Modell durchgeführt. Für diese 6 Analysen wurden die durchschnittliche Metalldispersion und die Standardabweichung in Tabelle 1 angegeben.
Tabelle 1. Wiederholbarkeitsergebnisse für sechs Analysen auf 0,5 %igem Platin-Aluminiumoxid unter Verwendung von CO undH2 als Prüfgase auf dem ChemiSorb Auto-Modell.
| 0,5% Pt-Al | RUN 1 | RUN 2 | RUN 3 | x̄ | σ |
| Metalldispersion (%), CO | 31.88 | 32.22 | 30.06 | 31.39 | 1.16 |
| Metalldispersion (%), H2 | 34.73 | 34.21 | 34.94 | 34.63 | 0.37 |
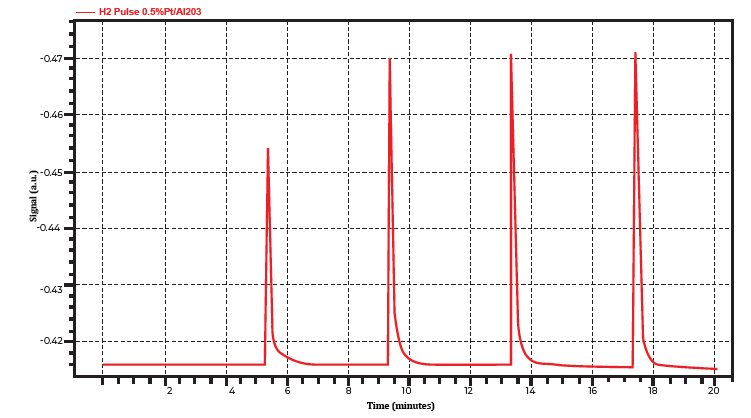
Abbildung 1A. Ein typisches Profil mit einem vollständig verbrauchten, einem teilweise verbrauchten und drei Sättigungspeaks unter Verwendung von 10 % H2/Ar als Prüfgas auf 0,5 % Platin-Aluminiumoxid.
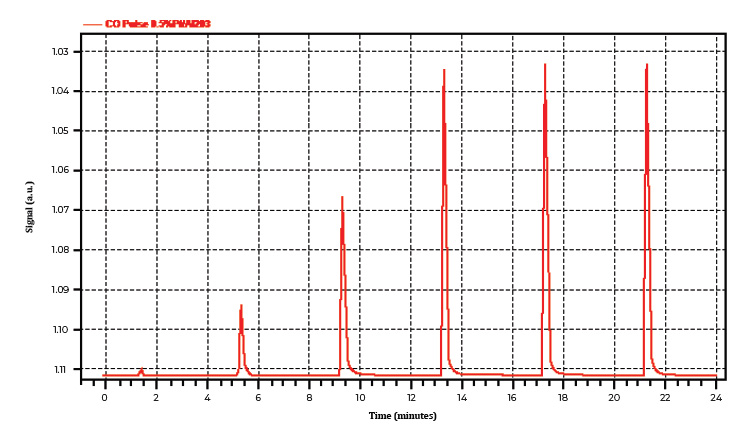
Abbildung 1B. Ein typisches Profil mit einem vollständig verbrauchten, zwei teilweise verbrauchten und drei Sättigungspeaks unter Verwendung von 10 % CO/He als Prüfgas auf 0,5 % Platin-Aluminiumoxid.
Eine Metallbeladung von 0,5 % Pt/Al2O3 bedeutet nicht, dass das gesamte Platin aktiv an chemischen Reaktionen beteiligt ist. Daher ist die Messung der Metalldispersion für die Bewertung der Aktivität eines Katalysators unerlässlich. So ergab die Impuls-Chemisorption in Versuch eins eine Dispersion von 31,39 %, was darauf hindeutet, dass nur 31,39 % des Platins zugänglich und aktiv an Oberflächenreaktionen beteiligt ist. Das restliche Platin kann in der Masse eingebettet oder in der Trägerstruktur eingeschlossen sein, so dass es für die katalytische Aktivität unzugänglich ist.
Die Methode der Katalysatorherstellung spielt eine wichtige Rolle bei der Bestimmung der Zugänglichkeit. In einigen Fällen können aktive Metallteilchen in den Träger eingebettet werden, wodurch einige der aktiven Stellen blockiert werden.
Das ChemiSorb Auto ist ein einzigartiges Instrument, das wertvolle Daten über den prozentualen Anteil der aktiven Spezies auf der Katalysatoroberfläche liefert. Ein höherer Metalldispersionswert korreliert im Allgemeinen mit einer größeren katalytischen Aktivität. Das Verständnis dieser Aktivität hilft Wissenschaftlern, fundierte Entscheidungen über die Steigerung der Produktion der gewünschten Produkte oder die Umgestaltung von Katalysatoren zur Verbesserung der Leistung zu treffen.