Introduction
Les processus de séparation sont un élément essentiel de l'industrie chimique. Les séparations oléfine/paraffine sont l'une des séparations les plus importantes au niveau industriel pour la production de plastiques. Au niveau mondial, 150 millions de tonnes d'éthylène et 130 millions de tonnes de propylène sont produites chaque année. L'adsorption modulée en pression, les séparations membranaires et la distillation cryogénique sont trois méthodes qui peuvent être utilisées pour séparer les oléfines des paraffines pour la production de plastiques.
La distillation cryogénique est la méthode la plus fréquemment utilisée pour la séparation de l'éthane et de l'éthylène. La distillation cryogénique sépare l'éthane et l'éthylène par leur différence de point d'ébullition. Le point d'ébullition de l'éthane est de -89°C et celui de l'éthylène de -103,7 °C. En raison de la similitude de ces points d'ébullition, la séparation de l'éthane et de l'éthylène par distillation cryogénique est extrêmement coûteuse, nécessitant généralement des centaines de plateaux dans une colonne de distillation pour obtenir la pureté nécessaire de l'éthylène en tant que produit.
La séparation de l'éthane et de l'éthylène à l'aide de membranes est réalisée à plus petite échelle que la distillation cryogénique. Une fois de plus, l'éthane et l'éthylène ont une taille et une forme similaires, ce qui rend la séparation difficile. Un gradient de pression important est nécessaire pour réussir à séparer les deux gaz. En outre, les performances de séparation d'une membrane ne permettent pas d'obtenir la même pureté d'éthylène que celle produite dans une colonne de distillation. Par conséquent, un traitement supplémentaire est généralement nécessaire pour obtenir la pureté souhaitée.
Les séparations basées sur l'adsorption, telles que l'adsorption par variation de pression, constituent la dernière méthode de séparation de l'éthane et de l'éthylène. L'adsorption modulée en pression nécessite moins d'énergie pour séparer l'éthane de l'éthylène que la distillation cryogénique. Cependant, comme pour les séparations par membrane, il est difficile d'obtenir la pureté souhaitée en une seule étape, de sorte que plusieurs colonnes d'adsorption sont nécessaires. Néanmoins, de nouveaux matériaux sont continuellement étudiés pour améliorer les performances de séparation de l'éthane et de l'éthylène par adsorption.
Expérimental
Le tamis moléculaire 5A a été utilisé pour les expériences de séparation par adsorption de l'éthane et de l'éthylène. Avant l'analyse, le MS 5A a été activé sous flux d'hélium pendant 1 heure à 100 °C, puis chauffé à 300 °C pendant 10 heures supplémentaires. On a ensuite laissé l'échantillon refroidir à température ambiante avant de commencer les mesures de percée.
La percée a été réalisée à 25 °C et à la pression atmosphérique en utilisant un débit équimolaire d'éthane (2 sccm) et d'éthylène (2 sccm) dans un gaz porteur d'hélium (15 sccm). L'argon (1 sccm) a été utilisé comme gaz traceur pour déterminer le début des mesures de percée. L'expérience a été considérée comme terminée lorsque la concentration mesurée à la sortie a atteint un équilibre. Après la percée, l'échantillon a été purgé sous flux d'hélium pendant 20 minutes avant d'être chauffé à 100 °C pour éliminer tout l'éthane ou l'éthylène adsorbé. Au total, trois mesures de percée ont été effectuées par cycle, avec une activation complète avant chaque cycle.
Résultats
Les courbes de rupture pour les trois expériences d'adsorption d'éthane-éthylène sur le tamis moléculaire 5A sont présentées dans la figure 1 ci-dessous.

Les trois mesures sont en accord et présentent des formes de pics qui sont cohérentes avec une adsorption compétitive entre l'éthane (adsorbant faible) et l'éthylène (adsorbant fort). L'enroulement de l'éthane est évident dans les courbes de percée et une quantité significative d'éthane est déplacée par l'adsorption de l'éthylène. La quantité d'éthane adsorbée à l'équilibre était d'environ 0,3 mmol/g et la quantité d'éthylène adsorbée à l'équilibre était d'environ 1,9 mmol/g, ce qui donne une sélectivité comprise entre 5,5 et 6,5 pour les trois mesures.
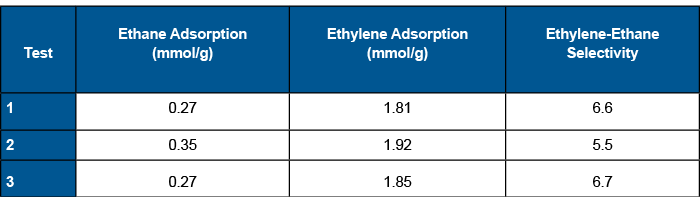
Lors des expériences de percée, l'argon (gaz traceur) perce en premier, suivi de l'éthane. La concentration d'argon diminue lors de la percée de l'éthane car la concentration du gaz de sortie change. Au début de l'expérience, seuls l'argon et l'hélium, le gaz porteur, sont acheminés vers le spectromètre de masse. Une fois que l'éthane a percé, l'argon, l'hélium et l'éthane atteignent tous le spectromètre de masse. Au départ, la concentration d'éthane à la sortie est supérieure à la concentration d'alimentation en raison de l'enroulement. La concentration d'éthane chute jusqu'à la concentration d'alimentation une fois que l'éthylène atteint la saturation. À ce moment-là, toutes les espèces ont atteint l'équilibre et l'expérience de percée est terminée. Le tableau 1 ci-dessous indique les quantités adsorbées à l'équilibre pour l'éthane et l'éthylène, ainsi que la sélectivité pour les trois expériences.
Conclusion
Le tamis moléculaire 5A est un adsorbant efficace pour la séparation de l'éthylène de l'éthane, atteignant une sélectivité d'environ 6,5 dans ces études de rupture. En outre, nous avons déterminé que la quantité d'adsorption d'éthylène à l'équilibre était de 1,9 mmol/g.