Introducción
Los procesos de separación son un componente fundamental de la industria química. Las separaciones de olefinas y parafinas son una de las más importantes desde el punto de vista industrial para la producción de plásticos. En todo el mundo se producen cada año 150 millones de toneladas métricas de etileno y 130 millones de toneladas métricas de propileno. La adsorción por cambio de presión, las separaciones por membrana y la destilación criogénica son tres métodos que pueden utilizarse para separar las olefinas de las parafinas para la producción de plásticos.
La destilación criogénica es el método más utilizado para la separación del etano y el etileno. La destilación criogénica separa el etano y el etileno por su diferencia de puntos de ebullición. El etano tiene un punto de ebullición de -89 °C y el etileno tiene un punto de ebullición de -103,7 °C. Debido a la similitud de estos puntos de ebullición, la separación del etano y el etileno mediante destilación criogénica es extremadamente costosa, ya que suele requerir cientos de bandejas en una columna de destilación para alcanzar la pureza necesaria del etileno como producto.
Las separaciones de etano y etileno mediante membranas se realizan a menor escala que la destilación criogénica. Una vez más, el etano y el etileno son similares en tamaño y forma, lo que dificulta la separación. Se requiere un gran gradiente de presión para separar con éxito los dos gases. Además, el rendimiento de separación de una membrana no es capaz de alcanzar la misma pureza de etileno que puede producirse en una columna de destilación. Por lo tanto, generalmente se requiere un procesamiento adicional para alcanzar la pureza deseada.
Las separaciones basadas en la adsorción, como la adsorción por oscilación de presión, es el último método de separación del etano y el etileno. La adsorción por oscilación de presión requiere menos energía para separar el etano del etileno que la destilación criogénica. Sin embargo, al igual que las separaciones por membrana, es difícil conseguir la pureza deseada en un solo paso, por lo que son necesarias varias columnas de adsorción. No obstante, se investigan continuamente nuevos materiales para mejorar el rendimiento de la separación basada en la adsorción para el etano y el etileno.
Experimental
Para los experimentos de separación por adsorción etano-etileno se utilizó el tamiz molecular 5A. Antes del análisis, el tamiz molecular 5A se activó bajo flujo de helio durante 1 hora a 100 °C, seguido de un calentamiento a 300 °C durante 10 horas más. A continuación, se dejó enfriar la muestra a temperatura ambiente antes de iniciar las mediciones de ruptura.
La ruptura se realizó a 25 °C y presión atmosférica utilizando un caudal equimolar de etano (2 sccm) y etileno (2 sccm) en un gas portador de helio (15 sccm). Se utilizó argón (1 sccm) como gas trazador para determinar el inicio de las mediciones de ruptura. El experimento se consideró completo cuando la concentración de salida medida alcanzó un equilibrio. Tras la penetración, se dejó purgar la muestra bajo flujo de helio durante 20 minutos antes de calentarla a 100 °C para eliminar todo el etano o etileno adsorbido. Se realizaron un total de tres mediciones de penetración en ciclos con activación completa antes de cada ciclo.
Resultados
En la figura 1 se muestran las curvas de avance de los tres experimentos de adsorción de etano-etileno en el tamiz molecular 5A.

Las tres mediciones concuerdan y muestran formas de pico que concuerdan con la adsorción competitiva entre etano (adsorbente débil) y etileno (adsorbente fuerte). El roll-up de etano es evidente en las curvas de ruptura y una cantidad significativa de etano es desplazada por la adsorción de etileno. La cantidad de equilibrio de etano adsorbido fue de aproximadamente 0,3 mmol/g y la cantidad de equilibrio de etileno adsorbido fue de aproximadamente 1,9 mmol/g, lo que dio como resultado una selectividad de entre 5,5 y 6,5 en las tres mediciones.
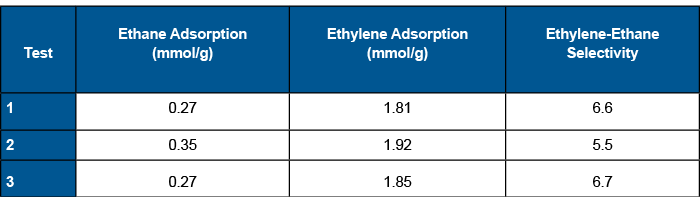
Durante los experimentos de penetración, el argón (gas trazador) penetra primero, seguido del etano. La concentración de argón disminuye con la penetración del etano porque cambia la concentración del gas de salida. Al principio del experimento, sólo el argón y el gas portador helio fluyen hacia el espectrómetro de masas. Una vez que el etano penetra, el argón, el helio y el etano llegan al espectrómetro de masas. Inicialmente, la concentración de etano de salida es superior a la concentración de alimentación debido al rollup. La concentración de etano desciende hasta la concentración de alimentación después de que el etileno alcance la saturación. En este momento, todas las especies han alcanzado el equilibrio y el experimento de ruptura se ha completado. La Tabla 1 muestra las cantidades de equilibrio adsorbidas de etano y etileno, así como la selectividad en los tres experimentos.
Conclusión
El tamiz molecular 5A es un adsorbente eficaz para la separación del etileno del etano, alcanzando una selectividad de aproximadamente 6,5 en estos estudios de avance. Además, determinamos que la cantidad de adsorción de etileno en equilibrio era de 1,9 mmol/g.