Einführung
Die Chemisorption ist ein wichtiges Analyseverfahren zur Untersuchung der Oberflächeneigenschaften von Feststoffen, insbesondere im Bereich der Katalyse. Im Gegensatz zur Physisorption, bei der schwache van-der-Waals-Kräfte wirken und die in der Regel reversibel ist, sind bei der Chemisorption starke, spezifische Wechselwirkungen wie kovalente oder ionische Bindungen erforderlich. Diese Wechselwirkungen führen häufig zur Bildung einer Monoschicht und sind im Allgemeinen irreversibel, was die Chemisorption sehr selektiv und informativ für die Oberflächencharakterisierung macht.
Während die Physisorption in der Regel zur Bestimmung der Oberfläche und der Porenstruktur verwendet wird, bieten Chemisorptionsverfahren wichtige Einblicke in die Anzahl, Art und Stärke der aktiven Stellen auf Katalysatoroberflächen. Diese Informationen sind für die Bewertung der Metalldispersion, der Adsorptionsstärke und der katalytischen Reaktivität von entscheidender Bedeutung; dies sind Schlüsselparameter für die Entwicklung und Optimierung von Katalysatoren.
Arbeitsprinzip der temperaturprogrammierten Reduktion
Die temperaturprogrammierte Reduktion (TPR) gilt als die am häufigsten verwendete Chemisorptionsmethode zur Charakterisierung der Reduzierbarkeit von Metalloxiden. Sie liefert Informationen wie die Oxidationsstufen der Metalloxide und die Stärke der Metall-Träger-Wechselwirkungen. Die Kenntnis der Temperatur, bei der das Metalloxid vollständig reduziert wird, gibt Aufschluss über die Aktivierung des Katalysators. In einem TPR-Profil entspricht die Anzahl der Reduktionsspitzen den Oxidationszuständen. Die Fläche unter dem Peak kann zur Quantifizierung des Wasserstoffverbrauchs verwendet werden.
Das Funktionsprinzip der temperaturgesteuerten Reduktion ist recht einfach. Ein 10%igesH2/Ar-Gasgemisch strömt durch das Probenbett, während die Temperatur linear ansteigt. Der Wasserstoff reduziert die Metalloxide zu Metallen und erzeugt Wasser. Ein Slush-Bad, eine Mischung aus flüssigem Stickstoff (LN2) und Isopropylalkohol (IPA), wurde verwendet, um Feuchtigkeit aus der Reaktion abzufangen. Am Beispiel von Kupferoxid wird gezeigt, wie Kupferoxid mit Wasserstoff reagiert und dabei Kupfer und Wasser erzeugt. Abbildung 1 zeigt ein Kupferoxid-TPR-Profil.
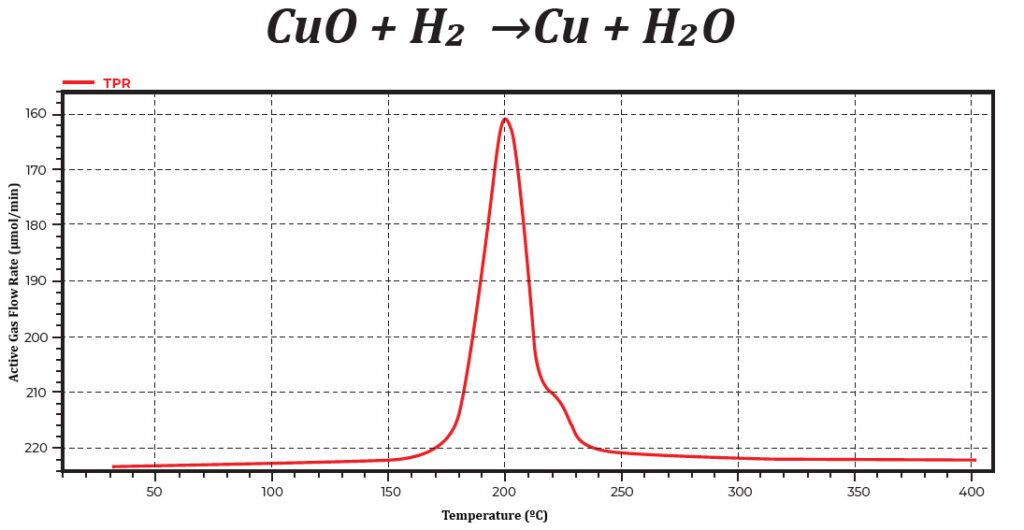
Abbildung 1. Temperaturprogrammiertes Reduktionsprofil von Kupferoxid. Die aktive Gaskonzentration ist als Funktion der Temperatur dargestellt.
Es wurden drei Analysen mit ChemiSorb Auto durchgeführt. Die Ergebnisse lagen innerhalb der im Standardmaterialheft angegebenen Spezifikation
. Tabelle 1 zeigt den Durchschnitt und die Standardabweichung
dieser Analysen.
| CuO | RUN 1 | RUN 2 | RUN 3 | x̄ | σ |
| Spitzentemperatur (°C) | 195.90 | 195.70 | 200.00 | 197.20 | 2.43 |
| H2-Verbrauch (cc/g) | 27.79 | 29.32 | 30.04 | 29.05 | 1.15 |
Mechanismus der Reduktion
Die Form des Peaks gibt Aufschluss über die Partikelgröße. Es gibt zwei Reduktionsmechanismen [1] (Abbildung 2), die für die Interpretation der TPR-Profile relevant sind. Bei sehr kleinen und feinen Partikeln kannH2 die Reduktion schnell einleiten, indem es die ersten Kerne bildet. Dieser Prozess läuft schnell ab und führt zu einer scharfen und symmetrischen Spitze im TPR-Profil. Diese Art von Verhalten ist charakteristisch für den Keimbildungsmechanismus.
In anderen Fällen können größere Katalysatorteilchen vorhanden sein. WennH2-Gas über die Oberfläche strömt und die Temperatur linear ansteigt, beginnt die Reduktion an der äußeren Hülle des Partikels.H2 muss dann nach innen diffundieren, um die nachfolgenden Schichten zu erreichen, was eine Diffusionsbeschränkung mit sich bringt und zu einem langsameren Gesamtreduktionsprozess führt.
Dieses Phänomen äußert sich in der Regel durch eine breitere und größere Spitze im TPR-Profil, auf die möglicherweise eine Verschiebung der Reduktionstemperatur folgt. Diese Art von Verhalten wird durch das Modell der "kontrahierenden Kugel" beschrieben.
Aus der Analyse der Form des TPR-Profils lassen sich qualitative Informationen über die Partikelgröße ableiten. Bei katalytischen Anwendungen sind im Idealfall kleine, fein verteilte Partikel auf der Oberfläche des Trägers vorhanden, um ihre Zugänglichkeit und Reaktivität bei chemischen Reaktionen zu maximieren.
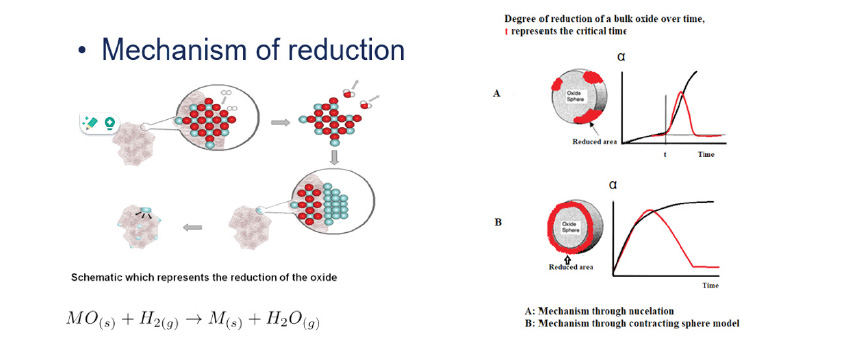
Abbildung 2. Modelle für den Mechanismus der Partikelzerkleinerung.
Wirkung von Promotoren
Die TPR bietet sowohl quantitative Daten als auch qualitative Einblicke in das Aktivierungsverhalten des Katalysators. Das Auftreten eines Reduktionspeaks im TPR-Profil wird im Allgemeinen als Indikator für die Katalysatoraktivierung interpretiert. Die Reduktionstemperatur selbst liefert jedoch wichtige Informationen, die bei der Entwicklung des Katalysators berücksichtigt werden sollten.
Wenn ein fein dispergierter Katalysator zur Aktivierung eine hohe Temperatur benötigt, besteht ein erhöhtes Risiko des Sinterns. Das Sintern führt zu einer Verringerung der metallischen aktiven Oberfläche, wodurch sich die Zahl der verfügbaren aktiven Stellen für chemische Reaktionen verringert. Dieser Prozess läuft nicht spontan ab und führt in der Regel zu einem Verlust der katalytischen Aktivität.
Abbildung 3 zeigt beispielsweise eine Verschiebung der Reduktionstemperatur von CuO in Abhängigkeit von der Palladiumladung (Pd). Wie gezeigt, senkt eine Erhöhung des Pd-Gehalts die Reduktionstemperatur, was als vorteilhaft angesehen wird. Die Aktivierung eines Katalysators bei niedrigeren Temperaturen trägt dazu bei, die Dispersion zu erhalten und das Risiko des Sinterns zu verringern.
Die wichtigste Erkenntnis ist, dass die TPR ein wichtiges Instrument für die Charakterisierung von Katalysatoren ist. Sie ermöglicht es den Wissenschaftlern zu bewerten, wie effektiv der Träger die aktiven Spezies unter erhöhten Temperatur- und Druckbedingungen stabilisiert.
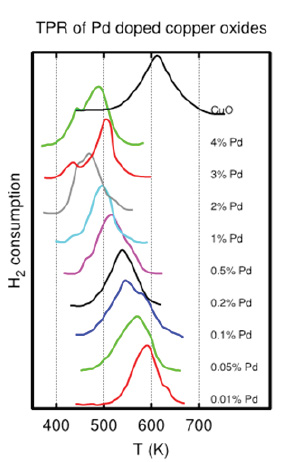
Abbildung 3. Auswirkung der unterschiedlichen Beladung von Promotoren auf CuO.
Automatische Gaskalibrierung
Das ChemiSorb Auto verfügt über ein patentiertes Mischventil, mit dem der Benutzer automatisch Gaskalibrierungen durchführen kann. Eine Gaskalibrierung ist erforderlich, um den Mengenverbrauch vonH2 zu quantifizieren. Diese Kalibrierung erfolgte automatisch durch Mischen von reinem Argon und reinem Wasserstoff, wobei das Wasserstoffverhältnis in einem elfstufigen Prozess von 10 % auf 0 % eingestellt wurde. Abbildung 4 zeigt einH2/Ar-Gaskalibrierungsprofil.
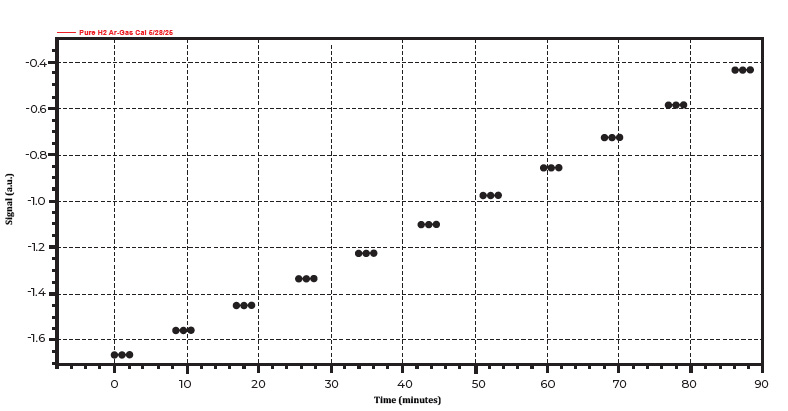
Abbildung 4. Ein typisches Gaskalibrierungsprofil für ein TPR-Experiment.
Die Gaskalibrierung kann entweder vor oder nach der Analyse durchgeführt werden. Eine neue Kalibrierung ist nicht
für jede neue Analyse erforderlich, es sei denn, die Analysebedingungen, wie z. B. Gaskonzentrationen oder
Durchflussraten, unterscheiden sich von denen, die bei der zuvor erstellten Kalibrierung verwendet wurden. In solchen Fällen gewährleistet eine neue
Kalibrierung Genauigkeit und Konsistenz unter den aktualisierten Bedingungen.
Referenz
Webb, P; Orr, C; Yunes, S. Analytical. Med. Tech, 1. Aufl. Micromeritics Instrument
Corp, 1997; S. 232-234.