Introduction
La chimisorption est une technique analytique essentielle utilisée pour étudier les propriétés de surface des matériaux solides, en particulier dans le domaine de la catalyse. Contrairement à la physisorption, qui implique de faibles forces de van der Waals et est généralement réversible, la chimisorption implique des interactions fortes et spécifiques telles que la liaison covalente ou ionique. Ces interactions aboutissent souvent à la formation d'une monocouche et sont généralement irréversibles, ce qui rend la chimisorption très sélective et instructive pour la caractérisation des surfaces.
Alors que la physisorption est couramment utilisée pour déterminer la surface et la structure des pores, les techniques de chimisorption fournissent des informations essentielles sur le nombre, la nature et la force des sites actifs à la surface des catalyseurs. Ces informations sont essentielles pour évaluer la dispersion des métaux, la force d'adsorption et la réactivité catalytique, des paramètres clés dans la conception des catalyseurs et l'optimisation des performances.
Principe de fonctionnement de la réduction programmée en température
La réduction programmée en température (RPT) est considérée comme la technique de chimisorption la plus couramment utilisée pour caractériser la réductibilité des oxydes métalliques. Elle fournit des informations telles que l'état d'oxydation des oxydes métalliques et la force des interactions métal-support. Le fait de savoir à quelle température l'oxyde métallique est complètement réduit fournit des informations sur l'activation du catalyseur. Dans un profil TPR, le nombre de pics de réduction correspond aux états d'oxydation. L'aire sous le pic peut être utilisée pour quantifier la quantité d'hydrogène consommée.
Le principe de fonctionnement de la réduction programmée en fonction de la température est assez simple. Un mélange de 10 % de gazH2/ Ar traverse le lit d'échantillons tandis que la température augmente de façon linéaire. L'hydrogène réduit les oxydes métalliques en métaux et produit de l'eau. Un bain de boue, mélange d'azote liquide (LN2) et d'alcool isopropylique (IPA), a été utilisé pour piéger l'humidité de la réaction. Si l'on prend l'exemple de l'oxyde de cuivre, celui-ci réagit avec l'hydrogène pour produire du cuivre et de l'eau. La figure 1 montre un profil TPR de l'oxyde de cuivre.
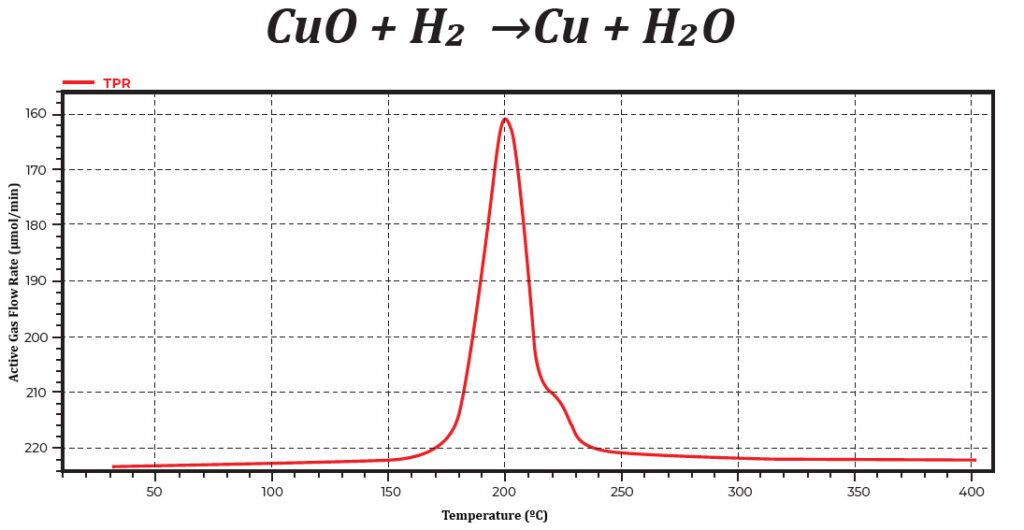
Figure 1. Profil de réduction de l'oxyde de cuivre programmé en fonction de la température. La concentration en gaz actif est indiquée en fonction de la température.
Trois analyses ont été effectuées à l'aide du ChemiSorb Auto. Les résultats étaient conformes aux spécifications
indiquées dans le livret du matériel standard. Le tableau 1 présente la moyenne et l'écart-type
de ces analyses.
| CuO | RUN 1 | RUN 2 | RUN 3 | x̄ | σ |
| Température de pointe (°C) | 195.90 | 195.70 | 200.00 | 197.20 | 2.43 |
| Consommation de H2 (cc/g) | 27.79 | 29.32 | 30.04 | 29.05 | 1.15 |
Mécanisme de réduction
La forme du pic fournit des informations sur la taille des particules. Il existe deux mécanismes de réduction [1] (figure 2) pertinents pour l'interprétation des profils TPR. Dans le cas de particules très petites et très fines,H2 peut rapidement initier la réduction en formant les premiers noyaux. Ce processus se produit rapidement, entraînant un pic net et symétrique dans le profil TPR. Ce type de comportement est caractéristique du mécanisme de nucléation.
Dans d'autres cas, des particules de catalyseur plus grosses peuvent être présentes. Lorsque le gazH2 s'écoule sur la surface à mesure que la température augmente linéairement, la réduction commence au niveau de l'enveloppe extérieure de la particule. L'H2 doit ensuite diffuser vers l'intérieur pour atteindre les couches suivantes, ce qui introduit une limitation de la diffusion et entraîne un processus de réduction global plus lent.
Ce phénomène se manifeste généralement par un pic plus large et plus important dans le profil TPR, qui est potentiellement suivi d'un déplacement de la température de réduction. Ce type de comportement est décrit par le modèle de la "sphère de contraction".
En analysant la forme du profil TPR, on peut déduire des informations qualitatives sur la taille des particules. Dans les applications catalytiques, le scénario idéal implique des particules petites et finement dispersées à la surface du support, maximisant leur accessibilité et leur réactivité dans les réactions chimiques.
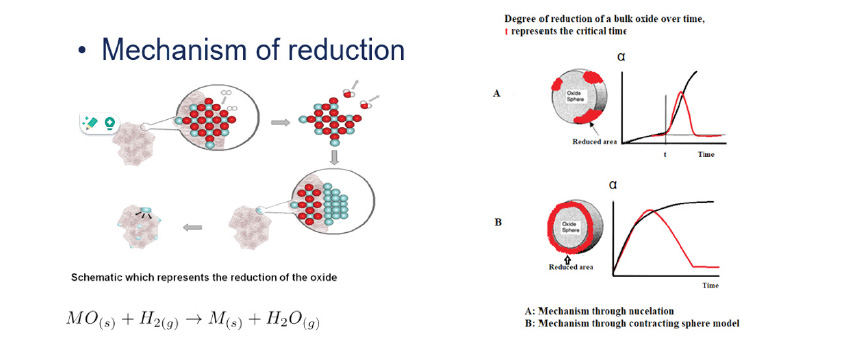
Figure 2. Modèles de mécanismes de réduction de la taille des particules.
Effet des promoteurs
Le TPR fournit à la fois des données quantitatives et des indications qualitatives sur le comportement d'activation du catalyseur. L'apparition d'un pic de réduction dans le profil TPR est généralement interprétée comme un indicateur de l'activation du catalyseur. Cependant, la température de réduction elle-même fournit des informations critiques qui doivent être prises en compte lors de la conception du catalyseur.
Si un catalyseur finement dispersé doit être activé à une température élevée, le risque de frittage augmente. Le frittage entraîne une réduction de la surface métallique active, ce qui réduit le nombre de sites actifs disponibles pour les réactions chimiques. Ce processus n'est pas spontané et entraîne généralement une perte d'activité catalytique.
Par exemple, la figure 3 montre un changement de la température de réduction du CuO en fonction de la charge de palladium (Pd). Comme on le voit, l'augmentation de la teneur en Pd abaisse la température de réduction, ce qui est considéré comme favorable. L'activation d'un catalyseur à une température plus basse permet de préserver la dispersion et d'atténuer le risque de frittage.
Il en ressort que le TPR est un outil essentiel pour la caractérisation des catalyseurs. Il permet aux scientifiques d'évaluer l'efficacité avec laquelle le support stabilise les espèces actives dans des conditions de température et de pression élevées.
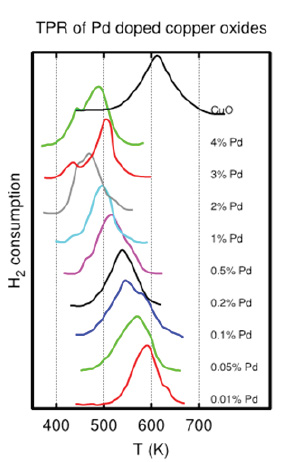
Figure 3. Effet de différentes charges de promoteurs sur le CuO.
Calibrage automatique du gaz
Le ChemiSorb Auto est équipé d'une vanne de mélange brevetée qui permet aux utilisateurs d'effectuer automatiquement des calibrages de gaz. Un étalonnage du gaz est nécessaire pour quantifier la consommation deH2. Ce calibrage a été effectué automatiquement en mélangeant de l'argon pur et de l'hydrogène pur, en ajustant le ratio d'hydrogène de 10% à 0% dans un processus en onze étapes. La figure 4 présente un profil d'étalonnage du gazH2/Ar.
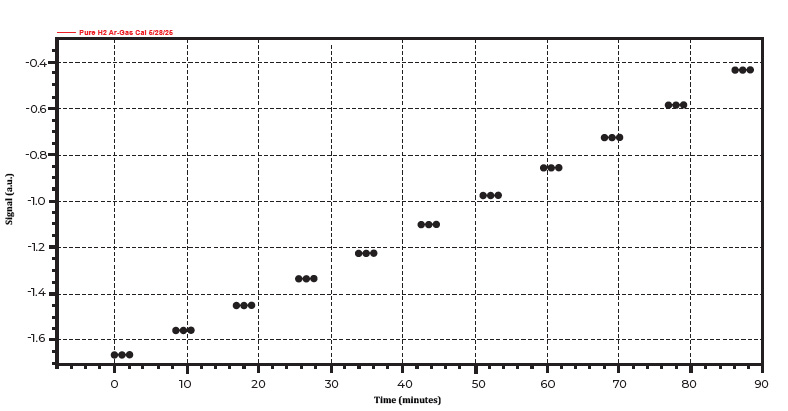
Figure 4. Profil d'étalonnage de gaz typique pour l'expérience TPR.
L'étalonnage des gaz peut être effectué avant ou après l'analyse. Un nouvel étalonnage n'est pas
nécessaire pour chaque nouvelle analyse, sauf si les conditions d'analyse telles que les concentrations de gaz ou
les débits diffèrent de celles utilisées dans l'étalonnage précédemment établi. Dans ce cas, un nouvel étalonnage
garantit la précision et la cohérence dans les nouvelles conditions.
Reference
Webb, P ; Orr, C ; Yunes, S. Analytical. Med. Tech, 1ère éd. Micromeritics Instrument
Corp, 1997 ; pp 232-234.