Abstrakt
Die chemische Adsorptionsisotherme gibt Aufschluss über die aktive Oberfläche eines Materials und wird seit vielen Jahren als analytisches Standardinstrument für die Bewertung von Katalysatoren eingesetzt. Seit den 1950er Jahren haben sich temperaturprogrammierte Reaktionstechniken als unverzichtbare Ergänzung zur Analyse der Chemisorptionsisotherme in vielen Bereichen von Industrie und Forschung etabliert. Dieses Papier bietet eine Einführung in diese Analysetechniken.
Einführung
Die optimale Gestaltung und effiziente Nutzung von Katalysatoren erfordert ein gründliches Verständnis der Oberflächenstruktur und der Oberflächenchemie des katalytischen Materials. Chemische Adsorptionsanalysen (Chemisorption) können einen Großteil der Informationen liefern, die zur Bewertung von Katalysatormaterialien in der Entwurfs- und Produktionsphase sowie nach einer gewissen Nutzungsdauer erforderlich sind. Die erforderlichen Analysegeräte sind relativ kostengünstig, einfach zu bedienen und schnell im Vergleich zu anderen Geräten, mit denen dieselben Informationen gewonnen werden können.
Unterscheidung zwischen physikalischer und chemischer Adsorption
Ein festes Material weist in der Regel eine heterogene Verteilung der Oberflächenenergie auf. Gas-, Dampf- oder Flüssigkeitsmoleküle können an die Oberfläche gebunden werden, wenn sie sich nahe genug kommen, um miteinander in Wechselwirkung zu treten. Die Erörterungen in diesem Papier beschränken sich auf die Adsorption (und Desorption) von Gasen oder Dämpfen an (oder von) festen Oberflächen. Der Festkörper wird als Adsorptionsmittel bezeichnet; das Gas- oder Dampfmolekül vor der Adsorption wird als Adsorptionsmittel und während der Bindung an die Festkörperoberfläche als Adsorbat bezeichnet.
Physikalische Adsorption ist das Ergebnis einer relativ schwachen Feststoff-Gas-Wechselwirkung. Es handelt sich um eine physikalische Anziehungskraft, die aus unspezifischen, relativ schwachen Van-der-Waal-Kräften und einer Adsorptionsenergie resultiert, die in der Regel 80 kJ/Mol nicht übersteigt, wobei die typischen Energien deutlich geringer sind. Physikalisch adsorbierte Moleküle können entlang der Oberfläche des Adsorptionsmittels diffundieren und sind in der Regel nicht an eine bestimmte Stelle der Oberfläche gebunden. Da sie nur schwach gebunden sind, lässt sich die physikalische Adsorption leicht umkehren.
Die Adsorption kann auch zu einem Oberflächenkomplex führen, einer Verbindung, die viel stärker ist als eine physikalische Bindung, mit Adsorptionswärmen von bis zu 600 kJ/mol für C-N-Bindungen und 800 kJ/mol für chemische Bindungen. Bei einer chemischen Bindung werden die Elektronen zwischen dem Adsorbat und dem Adsorptionsmittel geteilt, was als Bildung einer Oberflächenverbindung angesehen werden kann. Aufgrund der Bindungsstärke ist die chemische Adsorption nur schwer umkehrbar.
Die physikalische Adsorption findet auf allen Oberflächen statt, sofern die Temperatur- und Druckbedingungen günstig sind. Die Chemisorption hingegen ist sehr selektiv und findet nur zwischen bestimmten adsorptiven und adsorbierenden Spezies statt und nur dann, wenn die chemisch aktive Oberfläche von zuvor adsorbierten Molekülen gereinigt wurde.
Unter geeigneten Bedingungen kann die physikalische Adsorption dazu führen, dass die adsorbierten Moleküle mehrere Schichten bilden. Die Chemisorption findet im Normalfall nur so lange statt, wie das Adsorptionsmittel in direkten Kontakt mit der Oberfläche treten kann; es handelt sich also um einen einschichtigen Prozess. Ausnahmen können bestehen, wenn das Adsorptionsmittel sehr polar ist, wie z. B. NH3. Auf der Oberfläche kann gleichzeitig physikalische und chemische Adsorption stattfinden; eine Schicht von Molekülen kann auf einer darunter liegenden chemisorbierten Schicht physikalisch adsorbiert werden. Dieselbe Oberfläche kann bei einer bestimmten Temperatur eine physikalische und bei einer höheren Temperatur eine chemische Adsorption aufweisen. Beispielsweise wird Stickstoff bei der Temperatur von flüssigem Stickstoff (77 K) physikalisch an Eisen adsorbiert, aber bei 800 K, einem Energieniveau, das für physikalische Adsorptionsbindungen zu hoch ist, wird Stickstoff chemisch adsorbiert und bildet Eisennitrid (Moore).
Allgemeine Anwendungen der Gassorption als Analyseinstrument
Aus der Beobachtung des Adsorptionsprozesses lassen sich eine Reihe von Oberflächenmerkmalen bestimmen. Die Menge der von einer Oberfläche aufgenommenen Moleküle hängt von mehreren Variablen ab, u. a. von der Temperatur, dem Druck, der Verteilung der Oberflächenenergie sowie der Oberfläche und Porosität des Festkörpers. Die Beziehung zwischen der Menge der adsorbierten Moleküle und dem Druck bei konstanter Temperatur wird als Adsorptionsisotherme bezeichnet.
Physikalische Adsorptions- und Desorptionsisothermen sind wichtig für die Charakterisierung der gesamten Oberfläche. Die geringste Änderung in der Form der aufgezeichneten Isotherme ist ein Hinweis auf ein bestimmtes Oberflächenmerkmal. Die Analyse der physikalischen Adsorptionsisothermen gibt Aufschluss über die Gesamtoberfläche, das Volumen und die Fläche der Meso- und Mikroporen, das Gesamtporenvolumen, die Verteilung des Porenvolumens und der Porenfläche nach Porengröße und die Verteilung der Oberflächenenergie. Somit ist die physikalische Adsorption ein wichtiges Instrument für die Untersuchung von Katalysatoren, insbesondere für die Bewertung der Trägerstruktur.
Die chemische Adsorptionsisotherme bewertet ebenfalls die Oberfläche, ist aber insofern selektiv, als sie nur die aktiven Bereiche untersucht, d. h. diejenigen, die in der Lage sind, eine chemische Bindung mit dem adsorbierenden Gas oder Dampf einzugehen. Diese Selektivität betrifft sowohl das Sondenmolekül als auch die molekulare oder atomare Zusammensetzung des aktiven Materials, so dass die Auswahl der Sondenmoleküle bei Chemisorptionstests viel wichtiger ist. Obwohl isotherme Chemisorptionstests für die Charakterisierung aktiver Oberflächen wichtig sind, sind temperaturprogrammierte Tests noch wichtiger. Die Grundform der von diesen Tests erzeugten Daten ähnelt einem Chromatogramm von Temperatur und desorbierter Menge.
Katalysator-Grundlagen
Ein Katalysator beeinflusst die Geschwindigkeit einer chemischen Reaktion. "Geschwindigkeit" ist das wichtigste Wort in dieser Beschreibung, denn ein Katalysator kann keine Reaktion auslösen, die nach den Gesetzen der Thermodynamik nicht zulässig ist. Ein Katalysator kann nur die Geschwindigkeit erhöhen, mit der sich die Reaktion dem Gleichgewicht nähert.
Zu den heterogenen Katalysatoren gehören Metalle, Metalloxide und feste Säuren. Reine Metalle können als feste Katalysatoren verwendet werden oder als kleine Körner auf der Oberfläche eines Trägermaterials wie TiO2, ZrO2, Al2O3 oder SiO2 dispergiert sein. Bei der Herstellung eines Trägerkatalysators werden Vorstufen der aktiven Komponenten und gegebenenfalls Promotoren ausgewählt und in einem Lösungsmittel gemischt. Die Mischung bildet einen Niederschlag oder wird zur Beschichtung eines inerten Trägers oder zur Imprägnierung eines Trägers verwendet. Schließlich wird das aktive Metall oder der Vorläufer auf dem Träger dispergiert. Das Produkt wird getrocknet, mit einem Bindemittel oder Formgebungsmittel gemischt und dann gemahlen, pelletiert, extrudiert oder anderweitig geformt. Schließlich wird das Material kalziniert und durch Oxidation, Reduktion oder andere Mittel aktiviert.
Eine Art von trägerlosen Katalysatoren besteht aus reinem Metall. Raney-Metallkatalysatoren werden z. B. durch Auflösen einer Aluminium-Nickel-Legierung in einer Natriumhydroxidlösung hergestellt, die die Aluminiumkomponente auflöst. Das Endprodukt ist ein hochporöser aktiver Metall-"Schwamm", von dem alle anderen Gerüstmaterialien entfernt wurden. Ein anderer trägerloser Metallkatalysator wird durch Schmelzen oder Sintern von Metalloxiden mit Promotoren hergestellt, wodurch sich in der gesamten Metallmasse ein Netz von Poren bildet (van der Laan). Ein Beispiel hierfür ist ein Katalysator für die Ammoniak-Synthese aus geschmolzenem Eisen.
Zeolitische Katalysatoren bilden eine weitere Gruppe. Zeolithe sind hydratisierte Alumosilikate und werden in der chemischen Industrie und in Raffinerien häufig eingesetzt. Ihre Aktivität wird durch das Verhältnis von Siliziumdioxid zu Aluminiumoxid beeinflusst. Amorphe Siliziumdioxid-Tonerde-Katalysatoren haben eine geringere Aktivität als zeolithische Katalysatoren und werden bei milden Hydrocrackverfahren eingesetzt. Für das Cracken ist eine saure Oberfläche erforderlich, die mit den an die Aluminiumatome gebundenen Sauerstoffatomen verbunden ist.
Chemisorption und Katalysatoren
Der katalytische Prozess kann durch eine kurze Abfolge von Schritten wie folgt verallgemeinert werden. Nehmen wir an, die Reaktionsmoleküle A und B befinden sich in der Gasphase über einer festen Oberfläche, die ein Ensemble aktiver Metallstellen S trägt. Wenn das Molekül A chemisch an eine der aktiven Stellen adsorbiert wird, bildet sich ein Oberflächenkomplex A. Anschließend reagiert A mit B und bildet das Molekül A+B, das die Stelle verlässt und so die Stelle S regeneriert.
Damit eine Katalyse stattfinden kann, muss mindestens eines der Reaktionsmoleküle adsorbiert werden. Wäre die beschleunigte Reaktionsgeschwindigkeit lediglich auf die Konzentration der Moleküle an der Oberfläche zurückzuführen, würde die Katalyse durch die physikalische Adsorption der Reaktanten erfolgen. Die Chemisorption ist ein wesentlicher Schritt, bei dem das adsorbierte Molekül einen Zwischenkomplex auf der Oberfläche bildet, der für eine chemische Reaktion empfänglicher ist. Die Abhängigkeit der Katalyse von der Chemisorption ist einer der Gründe, warum die Chemisorption eine so aufschlussreiche Analysetechnik bei der Untersuchung der Katalyse ist - die Chemie, die bei der Anwendung des Katalysators stattfindet, wird direkt im Labor beobachtet.
Die Leistung eines Katalysators hängt von mehreren Variablen ab. Erstens müssen die Adsorptionsstellen sowohl zahlreich als auch für die Reaktionsmoleküle verfügbar sein. In einigen Fällen befinden sich die Körner des aktiven Metalls an der Oberfläche, aber es gibt auch Körner, die sich unter der Oberfläche befinden und für die Reaktanten nicht verfügbar sind. Adsorptionsstellen, die sich nur an der Oberfläche befinden, reichen nicht aus, um eine optimale Leistung zu gewährleisten. Beispielsweise können sich einige potenzielle Adsorptionsstellen tief in einer Mikropore befinden, die zu eng ist, als dass das Reaktionsmolekül eintreten oder das Reaktionsprodukt austreten könnte; in diesem Fall kann die Oberflächenstelle nicht aktiv an der Chemisorption beteiligt sein. In diesem Fall kann die Oberflächenstelle nicht aktiv an der Chemisorption teilnehmen. Eine Stelle könnte sich entlang eines gewundenen Pfades befinden, der den effizienten Fluss der Reaktanten zur aktiven Stelle und der Produkte von der Stelle weg behindert. Da viele aktive Metalle sehr teuer sind, besteht ein wichtiges Designkriterium darin, die Anzahl der aktiven Stellen pro Metalleinheit zu maximieren.
Die katalytische Aktivität hängt davon ab, wie schnell die Chemisorption erfolgt und wie stark die Chemisorptionsbindung (Energie) ist. Ist die Bindung zu schwach, kann das Molekül vor der Reaktion desorbieren; ist sie zu stark, kann sich die Freisetzung des Produkts und die Regeneration der Stelle verzögern. Isotherme Chemisorptionsmethoden sowie temperaturprogrammierte Chemisorptionsmethoden können zur Untersuchung der Oberflächenenergieverteilung verwendet werden.
Die oben beschriebene Chemisorption bezieht sich auf den Einsatz von Katalysatoren in verschiedenen Anwendungen. Die gleichen Reaktionen, nur in kleinerem Maßstab, können auch in einem Probenröhrchen unter kontrollierten Bedingungen ablaufen, so dass der Prozess untersucht werden kann. Dies ist die Chemisorption als analytische Technik. Chemisorptionsanalysen werden zur physikalischen Charakterisierung eines Katalysatormaterials, zur Bestimmung der relativen Effizienz eines Katalysators bei der Förderung einer bestimmten Reaktion, zur Untersuchung von Katalysatorvergiftungen und zur Überwachung des Abbaus der katalytischen Aktivität im Laufe der Nutzungsdauer eingesetzt. Unter den verschiedenen Instrumenten, die zur Analyse von Katalysatoren eingesetzt werden, sind Chemisorptionsverfahren die am häufigsten verwendeten.
Chemisorptionsinstrumente
Isotherme Chemisorptionsanalysen werden mit zwei Chemisorptionsverfahren durchgeführt: a) statische volumetrische Chemisorption und b) dynamische Chemisorption (strömendes Gas).
Die volumetrische Technik eignet sich für eine hochauflösende Messung der Chemisorptionsisotherme von sehr niedrigem Druck bis zum Atmosphärendruck bei praktisch jeder Temperatur von nahezu Umgebungstemperatur bis 1000+ oC. Kommerzielle Ausführungsformen dieser Technik sind fast ausschließlich automatisiert. Um eine hochauflösende Isotherme zu erhalten, sind viele, präzise Dosierungsschritte auf dem Weg zum Gleichgewichtspunkt und viele Druckschritte erforderlich, die ohne Automatisierung ein zeitaufwändiges und fehleranfälliges Verfahren darstellen würden.
Die (dynamische) Technik mit strömendem Gas arbeitet bei Umgebungsdruck. Nachdem die Probe gereinigt wurde, werden kleine Injektionen (Dosen) von genau bekannten Mengen an Adsorptionsmittel in Pulsen verabreicht, bis die Probe gesättigt ist, daher der Name "Puls-Chemisorption". Ein kalibrierter Wärmeleitfähigkeitsdetektor (TCD) überwacht die Menge des Adsorptionsmittels, die nicht von aktiven Metallen aufgenommen wird. Diese Menge wird von der injizierten Menge subtrahiert und ergibt die bei jeder Injektion adsorbierte Menge. Diese werden addiert, um die Kapazität der Probenmasse zu bestimmen. Die Injektionen können mit einer Spritze oder mit einem manuellen oder automatischen HPLC-Schleifeninjektionsventil erfolgen. Da der Endpunkt (Sättigung) der einzige gemessene Punkt ist, kann die Anzahl der Injektionen sehr gering sein, und es gibt keine Druckänderungen. Daher wird die Fließgastechnik häufig manuell durchgeführt, obwohl es auch automatisierte Geräte gibt.
In den letzten Jahrzehnten haben sich temperaturprogrammierte Chemisorptionsanalysatoren als äußerst wertvolle Werkzeuge zur Charakterisierung von Katalysatoren erwiesen. Die Methode wird manchmal einfach als temperaturprogrammierte Reaktionen bezeichnet und umfasst temperaturprogrammierte Desorption (TPD), temperaturprogrammierte Reduktion (TPR) und temperaturprogrammierte Oxidation (TPO). Die dynamische Chemisorptionsmethode eignet sich besonders für die Durchführung von Temperaturprogrammanalysen.
Chemisorptions-Analysen
Die Vielseitigkeit der Chemisorptionsmethode wird durch den Umfang der Informationen, die über ein Material gewonnen werden können, veranschaulicht. Ein Teil der Vielseitigkeit wurde in den obigen Ausführungen bereits deutlich. In den folgenden Abschnitten werden weitere Möglichkeiten erforscht.
In den folgenden Beispielen werden nur Katalysatoren betrachtet, die aus einer einzigen aktiven Spezies bestehen, um die Berechnungen zu vereinfachen. Bei Katalysatoren mit gemischten Metallen müssten in vielen der nachstehenden Gleichungen eine Reihe von Termen summiert werden, einer für jede adsorbierende Spezies und jeder Term gewichtet nach dem Anteil der Spezies an der Gesamtmenge.
Die Chemisorptionsisotherme
Eine Isotherme ist eine Reihe von Datenpunkten zwischen adsorbierter Menge und Druck, die den Adsorptionsprozess bei einer konstanten Temperatur charakterisieren. Um dies besser zu verstehen, betrachten Sie einen Reaktor mit konstantem Volumen V, der eine Probe und eine Menge von Gasmolekülen N enthält. Die Chemisorptionstheorie geht davon aus, dass die aktive Oberfläche eines Festkörpers eine feste Anzahl Ns von Adsorptionsstellen enthält und jeweils nur ein Molekül eine Stelle besetzen kann. Die Moleküle im Probenröhrchen, die um einen Adsorptionsplatz konkurrieren, stellen eine Konzentration C dar, die allgemein durch die Lösung des Gasgesetzes ausgedrückt werden kann, oder
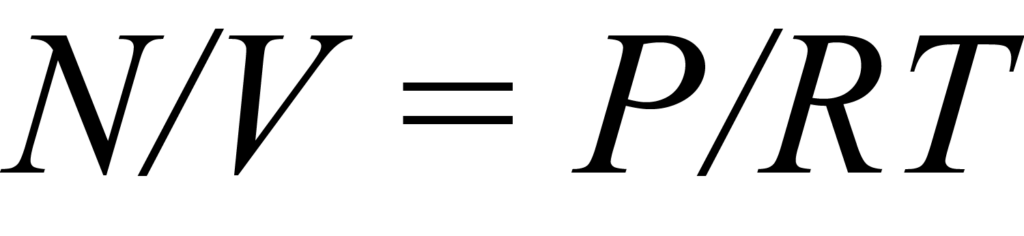
wobei N und V bereits definiert wurden, P der Druck, T die Temperatur und R die Gaskonstante ist.
Für ein bestimmtes Gas-Feststoff-System, das sich unter bestimmten Temperatur- und Druckbedingungen im Gleichgewicht befindet, wird ein bestimmter Anteil ϑ der Gesamtzahl der verfügbaren Plätze Ns von nads adsorbierten Molekülen besetzt. Dies wird beschrieben durch
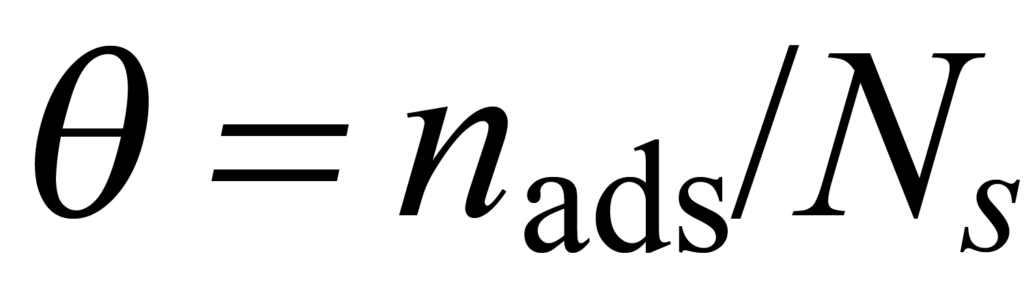
Die Geschwindigkeit, mit der das Gleichgewicht erreicht wird, hängt von der Konzentration der beteiligten Moleküle sowie von anderen Faktoren ab, die in einem Parameter zusammengefasst werden, der als "Geschwindigkeitskonstante" k bezeichnet wird.
Für den Adsorptionsprozess ist die Konzentration der nicht adsorbierten Moleküle, die um die verbleibenden Plätze konkurrieren, C-ϑC und die Adsorptionsrate ist kads(C-ϑC) oder kadsC(1-ϑ). Bei der Desorption ist der Anteil der desorbierten Moleküle ? und die Desorptionsrate ist kdesϑ. Wenn das Gleichgewicht erreicht ist, sind die Adsorptions- und die Desorptionsrate gleich, d. h.,
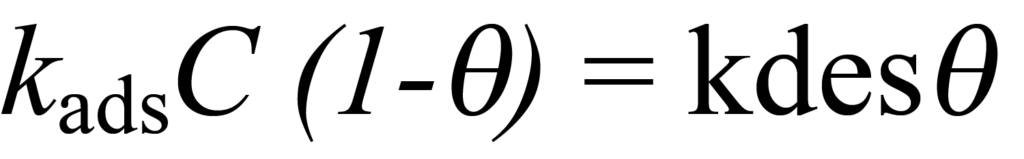
oder
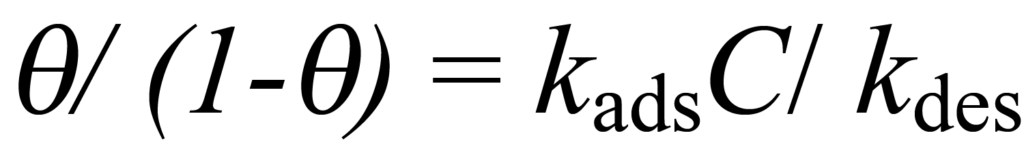
Die Verwendung von K zur Darstellung von kads/kdes und die Lösung für ϑ ergibt
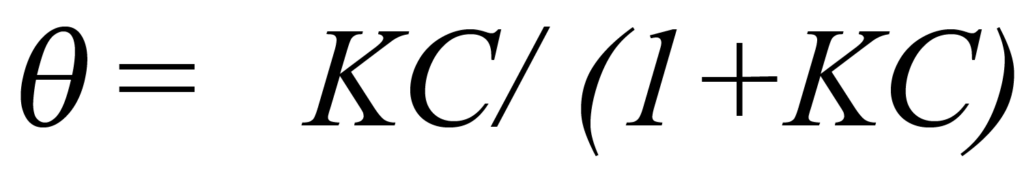
Wenn man davon ausgeht, dass die Umgebung ein konstantes Volumen V und eine konstante Temperatur T hat, ist eine Änderung des Drucks die einzige verbleibende Möglichkeit, die Konzentration C zu ändern. Gleichung 1 besagt, dass die Konzentration direkt proportional zum Druck ist; wenn also die Konzentrations-Druck-Proportionalitätskonstante mit K kombiniert und durch b dargestellt wird, kann Gleichung 4 geschrieben werden
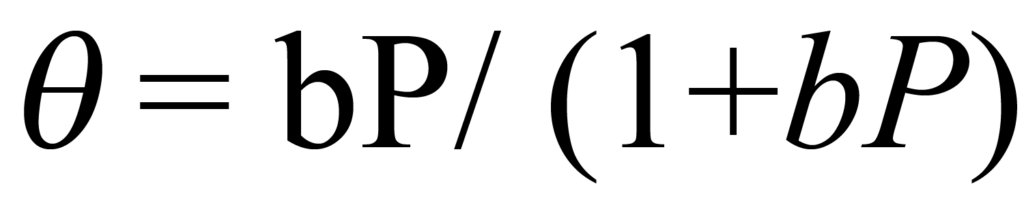
Dies ist die berühmte Langmuir-Isotherme, die die meisten Chemisorptionsisothermen genau beschreibt, bei denen es nicht zu einer Fragmentierung (Dissoziation) des adsorbierenden Moleküls kommt. Die Isotherme ist asymptotisch zu ϑ = 1, was eine vollständige Bedeckung oder Vervollständigung der Monolage bedeutet.
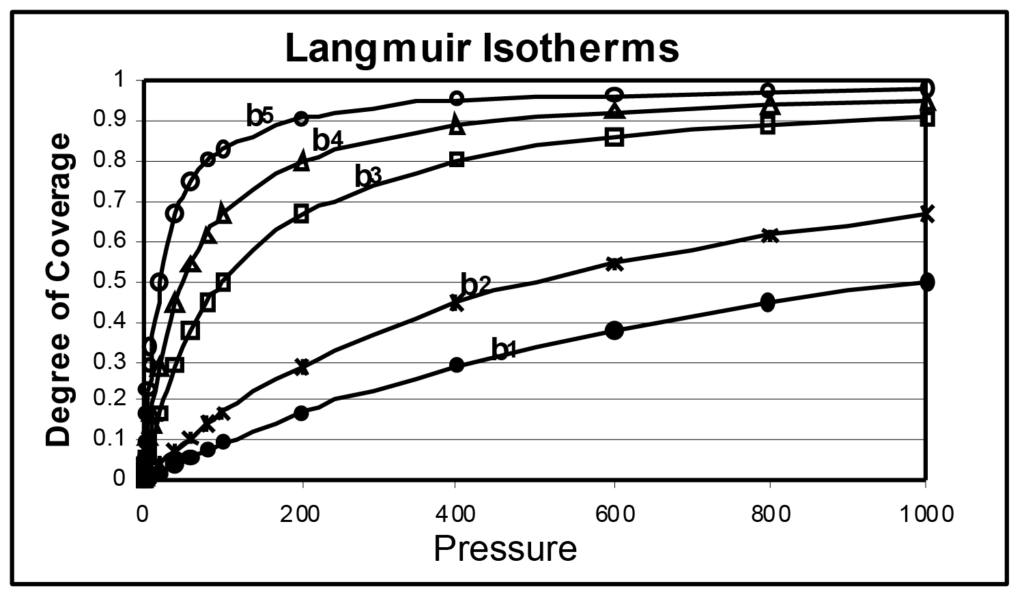
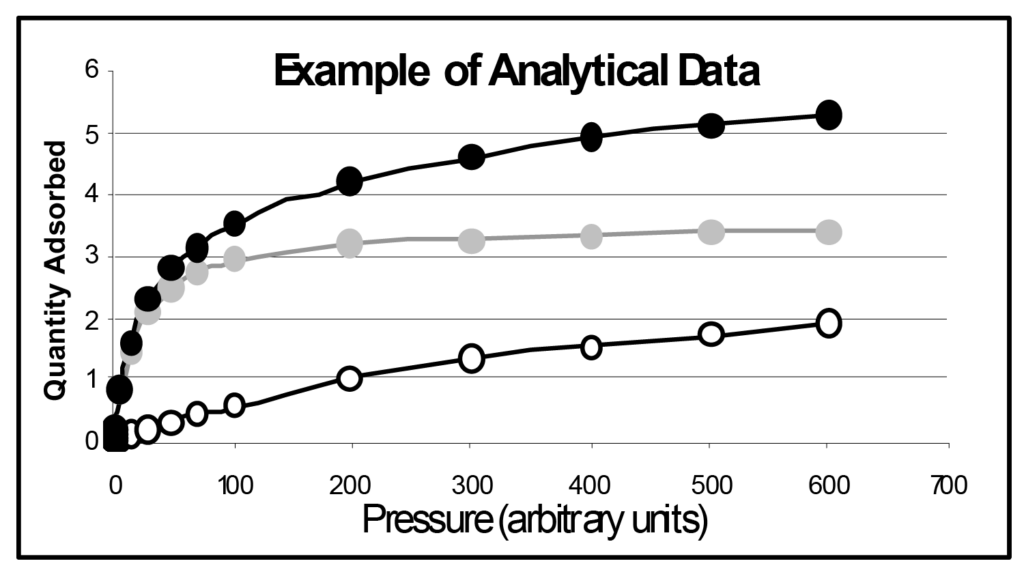
In Abbildung 1 sind mehrere Langmuir-Isothermen dargestellt, wobei der einzige Unterschied in der Größe von b besteht. Der Parameter b steht in direktem Zusammenhang mit der Oberflächenenergie; mit zunehmender Oberflächenenergie erhöht sich die Wahrscheinlichkeit der Adsorption bei einem bestimmten Druck. Der Parameter b steht in umgekehrter Beziehung zur Temperatur, die, wenn sie erhöht wird, die molekulare Energie erhöht und die Wahrscheinlichkeit der Adsorption bei einem gegebenen Druck verringert.
In der Abbildung ist b1 kleiner als b2, das wiederum kleiner als b3 ist, und so weiter, wobei b5 50 Mal größer als b1 ist. Daraus lässt sich ableiten, dass dieselbe Probe, die bei fünf verschiedenen Temperaturen analysiert wird, einen ähnlichen Satz von Isothermen ergeben würde, wie fünf verschiedene Proben mit unterschiedlicher Oberflächenenergie, die bei derselben Analysetemperatur gemessen werden.
Die Ermittlung einer Chemisorptionsisotherme ist nicht unbedingt eine direkte Messung, wie in Abbildung 2 dargestellt. Im typischen Fall, der in diesen Abbildungen dargestellt ist, gibt es Moleküle (gekennzeichnet durch R), die schwach an der Oberfläche des Trägers adsorbiert sind, und es gibt auch eine chemisorbierte Monoschicht von Molekülen (gekennzeichnet durch I) auf der aktiven Oberfläche. Je nach Druck und Temperatur können auch Moleküle physikalisch auf der chemisorbierten Monoschicht adsorbiert sein.
Schwache Adsorption wird als reversible Adsorption und starke Chemisorption als irreversible Adsorption bezeichnet, daher die Bezeichnungen R und I in der Abbildung. Die Ausgangsisotherme ist eine Kombination aus reversibler und irreversibler Adsorption.
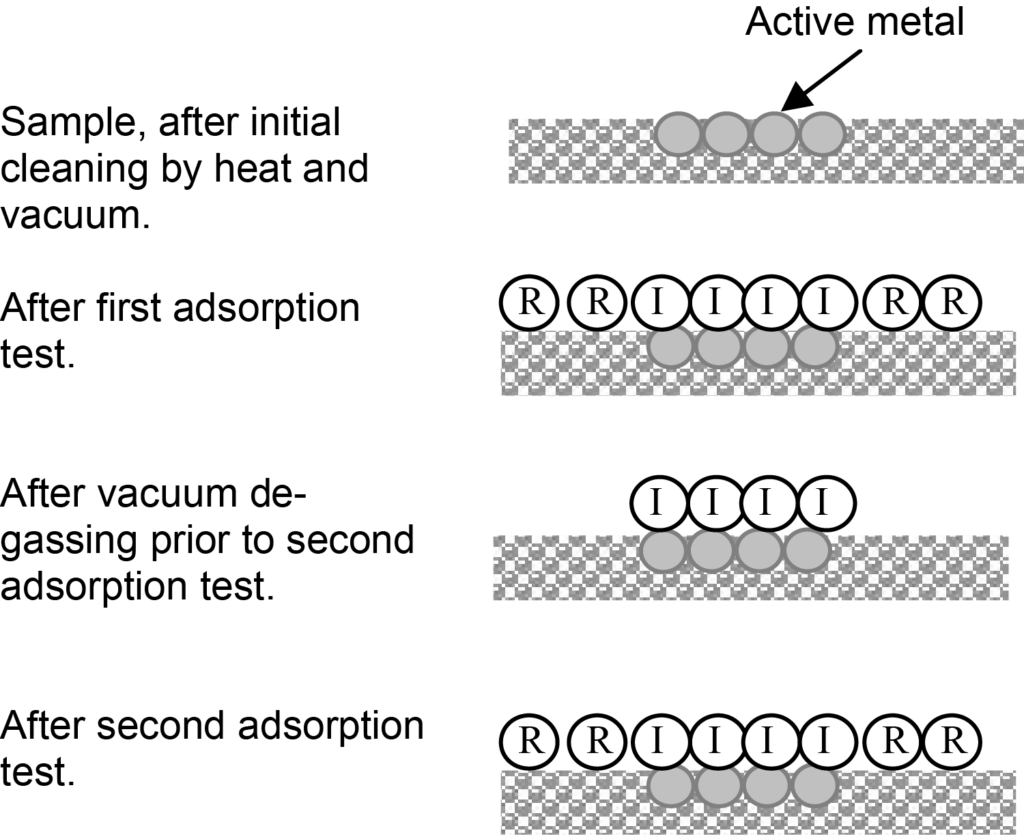
Die reversiblen und irreversiblen Beiträge zu einer kombinierten Isotherme können durch die Durchführung eines zweiten Adsorptionstests unterschieden werden. Nach dem ersten Adsorptionstest und vor dem zweiten Test wird die Probe nur dem Vakuum ausgesetzt, wodurch die schwach adsorbierten Moleküle desorbiert werden und nur die Moleküle übrig bleiben, die eine starke Chemisorptionsbindung mit der aktiven Oberfläche eingegangen sind.
Der zweite Adsorptionstest wird unter denselben Bedingungen wie der erste Test durchgeführt, aber diesmal ist die aktive Oberfläche bereits mit einer chemisorbierten Monolage bedeckt. Es wird nur die Menge an Adsorbat aufgenommen, die mit der reversiblen Adsorption verbunden ist. Subtrahiert man die reversibel adsorbierte Menge von der kombinierten Isotherme bei jedem Druckwert, erhält man eine Isotherme der ireversiblen Adsorption. Die analytischen Ergebnisse sind in Abbildung 3 dargestellt.
Anzahl der zugänglichen aktiven Standorte
Sowohl statische volumetrische als auch dynamische Chemisorptionsverfahren können zur Messung der Gasmenge verwendet werden, die erforderlich ist, um eine Monoschicht aus Chemisorbat auf einer aktiven Oberfläche zu bilden. Die dynamische Methode liefert nur einen einzigen Datenpunkt, der der Menge an Adsorptionsmittel entspricht, die erforderlich ist, um die aktive Oberfläche mit einer Monolage zu sättigen. Die Monolagenkapazität der aktiven Oberfläche wird aus der abgeleiteten irreversiblen Adsorptionsisotherme berechnet, die in Abbildung 3 dargestellt ist. Da die irreversible Adsorptionsisotherme asymptotisch zum Wert der Gesamtbedeckung (der aktiven Oberfläche) ist, wird das Plateau der Isotherme zurück zur y-Achse extrapoliert, um den Wert der Monolagenkapazität zu erhalten. Die Extrapolation des linearen Abschnitts der kombinierten reversiblen/irreversiblen Isothermen auf die y-Achse liefert ebenfalls einen angemessenen Wert für die Monoschichtbedeckungsgröße.
Bei der dynamischen Chemisorptionsmethode werden (manuell oder automatisch) kleine, genau bekannte Mengen des Adsorptionsmittels in einen Strom von inertem Trägergas injiziert, der durch das Probenbett fließt.
Der Partialdruck des Adsorptionsmittels steigt während des Impulses kurzzeitig über der Probe an, und die eingespritzte Gasmenge wird ganz oder teilweise adsorbiert. Nicht adsorbiertes Gas wird durch den Detektor geströmt und dort registriert. Anders als bei der statischen Methode (siehe oben) handelt es sich bei der Nettoadsorption nur um eine irreversible Adsorption, da der Partialdruck des Adsorptionsmittels in der Gasmasse nach dem Durchgang des Adsorptionsimpulses im Wesentlichen Null ist und entweichende, schwach adsorbierte Moleküle durch den Trägerstrom zum Detektor gespült werden.
Während sich die Monoschicht auf der aktiven Oberfläche bildet, wird immer weniger von dem injizierten Adsorptionsmittel von der Probe aufgenommen. Die Injektionen werden so lange fortgesetzt, bis die Probe gesättigt ist, was dadurch angezeigt wird, dass alle nachfolgenden Detektorpeaks die gleiche Größe haben. Die Ergebnisse eines solchen Tests sind in Abbildung 4 dargestellt, die das Ergebnis des Detektors veranschaulicht. Die Fläche jedes Peaks ist proportional zu der Menge der Injektion, die nicht adsorbiert wurde.
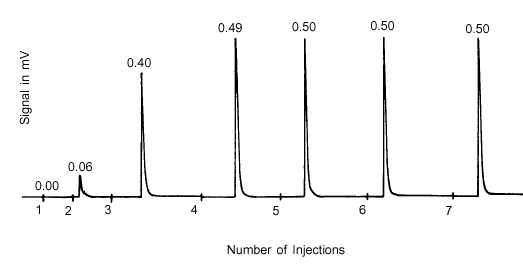
In Abbildung 4 zeigt die integrierte Fläche der mit den Injektionen 5, 6 und 7 verbundenen Peaks, dass keine Adsorption stattgefunden hat, so dass die aktive Fläche gesättigt ist. Die gesamte erste Injektion wurde adsorbiert, ebenso 88 % der Injektion 2, 20 % der Injektion 4 und 2 % der Injektion 3. Aus der bekannten Menge jeder Injektion, dem Anteil jeder Injektion, der adsorbiert wurde, und der Masse des Probenmaterials wird die Anzahl der Mole des adsorptiven Gases bestimmt, die von jedem Gramm der Probe aufgenommen wurden.
Der Adsorptionsprozess kann die Aufspaltung eines molekularen Adsorptionsmittels in zwei oder mehr molekulare oder atomare Einheiten (Ionen oder Radikale) beinhalten, wobei jede Einheit eine Bindung mit einzelnen aktiven Oberflächenstellen eingeht. Dies wird als dissoziative Adsorption oder Adsorption zweiter Ordnung bezeichnet, im Gegensatz zur Adsorption erster Ordnung oder nicht-dissoziativen Adsorption, bei der das adsorptive Molekül während der Adsorption intakt bleibt. Das Ergebnis der dissoziativen Adsorption ist, dass die Anzahl der adsorptiven MoleküleNm, die pro Gramm der Probe aufgenommen wurden, nicht der Anzahl der aktiven Oberflächenatome entspricht, die an der Chemisorption beteiligt waren.
Um die Anzahl der beteiligten Oberflächenatome zu bestimmen, muss die Stöchiometrie der Oberflächenreaktion berücksichtigt werden. Die Stöchiometrie bezieht sich auf das Verhältnis zwischen den Mengen der Stoffe, die in einer bestimmten chemischen Reaktion miteinander reagieren, und den Mengen der entstehenden Produkte. So kann beispielsweise ein Wasserstoffmolekül (H2) in zwei Wasserstoffatome dissoziieren und mit zwei Atomen der aktiven Oberfläche reagieren, wie es bei Pt der Fall ist. Die Anzahl der von der aktiven Oberfläche aufgenommenen Adsorptionsmoleküle muss also mit einem Stöchiometriefaktor Fs multipliziert werden (wobei Fs = 2 im Beispielsfall), um die Anzahl der Oberflächenatome Ns oder "Stellen" zu erhalten. Mathematisch gesehen,
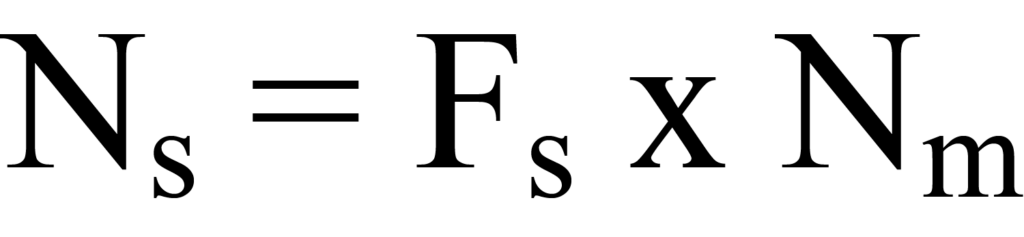
wobei Ns undNm pro Gramm der Probe bestimmt werden.
Das adsorptive Molekül kann sich in mehr als einer Konfiguration mit der aktiven Oberfläche verbinden. Der Anteil der Moleküle, die sich auf jede mögliche Weise binden, muss berücksichtigt werden, was häufig zu einem nicht ganzzahligen Stöchiometriefaktor führt.
Aktiver Oberflächenbereich
Die spezifische aktive Oberfläche ergibt sich aus der Anzahl der Moleküle Ns, die an der aktiven Oberfläche eines Gramms der Probe adsorbiert werden. Die spezifische aktive OberflächeAA wird durch Multiplikation der von einem Oberflächenmolekül belegten FlächeAm mit der Anzahl der adsorbierten Moleküle pro Gramm Ns bestimmt. Die von einem einzelnen Atom belegte Fläche, die aus dem Adsorptionsmittel stammt, kann in der Regel in der Literatur gefunden werden. Sie kann gegebenenfalls auch experimentell bestimmt werden, indem man die BET-Oberfläche einer Probe des reinen aktiven Materials mit N2 bestimmt und dann die molare Aufnahme des aktiven Adsorptionsmittels auf derselben Probe ermittelt.
Metalldispersion und prozentualer Metallanteil
Die Metalldispersion beschreibt das Verhältnis zwischen der Anzahl der für die Reaktion verfügbaren aktiven Metallatome und der Gesamtzahl der Metallatome im Katalysatormaterial. Die Menge an aktivem Metall pro Masseneinheit des Trägermaterials ergibt sich aus der Herstellungsformel; daraus ergibt sich die Menge der aktiven MetallatomeNT pro Masseneinheit des Katalysators. Die oben beschriebene Chemisorptionsanalyse dient zur Bestimmung der Menge an aktivem Metall pro Gramm, die für die Reaktion zur Verfügung steht. Die prozentuale Dispersion ist das Verhältnis der verfügbaren Menge zur Gesamtmenge der aktiven Moleküle mal 100 %, oder
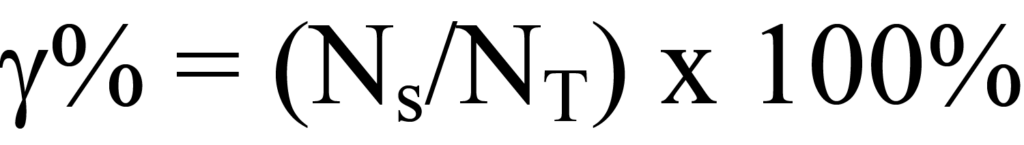
Die Dispersion wird als Verhältnis des verfügbaren Metalls zum Gesamtmetall ausgedrückt. Ein weiterer Anteil, der sich aus dem Herstellungsverfahren ergibt, ist das Verhältnis zwischen dem Gewicht des Metalls und der Masse des Katalysatormaterials, ausgedrückt als Dezimalbruch oder als Prozentsatz.
Aktive Partikel (Kristallit) Größe
Bei dieser Schätzung der aktiven Partikelgröße handelt es sich um eine geometrische Berechnung, die auf der Annahme beruht, dass die Kristallitform eine regelmäßige Geometrie aufweist, wobei in der Regel eine Kugel die Geometrie der Wahl ist. Aus früheren Berechnungen ist die aktive Oberfläche pro Gramm ProbenmaterialAA bekannt und aus dem Herstellungsverfahren des Katalysators der Anteil des Metalls in der Katalysatormasse.
Bei der Berechnung wird die Geometrie des Korns berücksichtigt. Ausgehend von der angenommenen regelmäßigen Geometrie kann der Durchmesser durch die Fläche und das Volumen ausgedrückt werden. Das Volumen des aktiven Metalls ist nicht bekannt, wohl aber die atomare oder molekulare Dichte ρm; daher kann das Volumen durch die Dichte ausgedrückt werden. Die Fläche des aktiven Metalls pro Gramm der Probe wurde zuvor gemessen, was einen Wert für die Fläche pro Masseneinheit des MetallsAm (m2/g) ergibt. Setzt man diese Ausdrücke in die allgemeine Beziehung für D = f(A,V) ein, erhält man
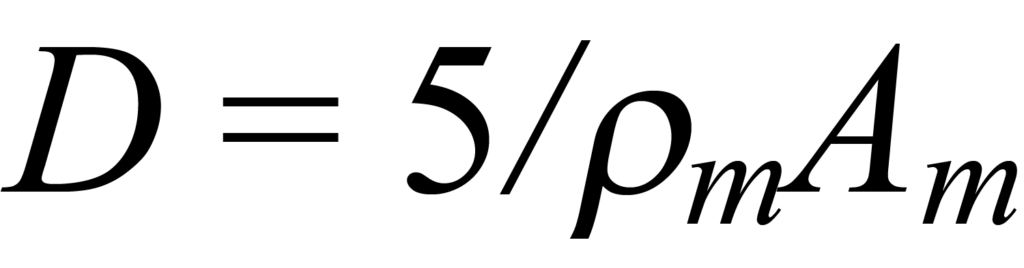
für ein kubisches Korn auf der Oberfläche (fünf von sechs Flächen freigelegt) und
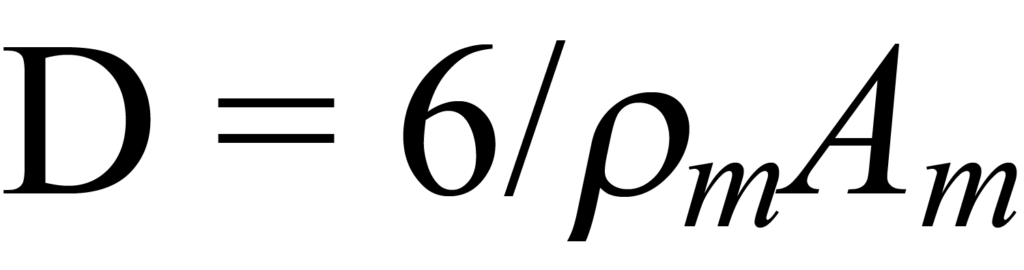
für ein halbkugelförmiges Teilchen.
Der nach der obigen Gleichung berechnete Durchmesser ist der durchschnittliche Durchmesser der aktiven Metallkörner, an denen die Adsorption stattgefunden hat.
Temperaturprogrammierte Chemisorption
Wie der Name der Methode schon sagt, ist die temperaturprogrammierte Chemisorption eine Methode, bei der die Auswirkungen der Temperatur auf Oberflächenreaktionen untersucht werden. Es gibt drei Hauptreaktionen, die in Abhängigkeit von der Temperatur untersucht werden: 1) Desorption, 2) Reduktion und 3) Oxidation.
Bei der temperaturprogrammierten Desorption nach der dynamischen Methode wird eine Probe in eine Probenzelle gegeben und vorbehandelt, um alle adsorbierten Stoffe von der aktiven Oberfläche zu entfernen. Anschließend wird ein ausgewähltes Gas oder ein Dampf an die aktiven Stellen chemisorbiert, bis eine Sättigung erreicht ist. Danach werden die verbleibenden Adsorptionsmoleküle mit einem Inertgas ausgespült. Die Temperatur (Energie) wird mit kontrollierter Geschwindigkeit erhöht, während ein konstanter Inertgasstrom über der Probe aufrechterhalten wird. Das Inertgas und alle desorbierten Moleküle werden mit einem TCD überwacht. Das TCD-Signal ist proportional zur Menge der desorbierten Moleküle, da die thermische Energie, die von einem Thermoelement überwacht wird, die Bindungsenergie überwindet. Die bei bestimmten Temperaturen desorbierten Mengen liefern Informationen über die Anzahl, Stärke und Heterogenität der Adsorptionsstellen. Die Analysedaten werden in der Regel als desorbierte Menge in Abhängigkeit von der Temperatur oder sowohl als Temperatur als auch als desorbierte Menge über der Zeit aufgetragen.
Abbildung 5 ist ein typisches TPD-Profil der Wasserstoffdesorption von Pt auf einem Al2O3-Träger. Der erste Peak wird bei einer Temperatur von 393 K erhalten. Dieser Peak entspricht der schwachen Adsorption von Wasserstoff und kann mit der Desorption vom Träger oder einer schwachen Chemisorption zusammenhängen. Der zweite Peak, der bei der nächsthöheren Temperatur (493 K) erhalten wird, entspricht wahrscheinlich einem Wasserstoffüberlauf aufgrund der Anwesenheit von Pt auf Aluminiumoxid. Der dritte und letzte Peak, der bei 570 K auftritt, entspricht dem durch Pt chemisorbierten Wasserstoff. Dieser Peak wird quantifiziert, um die Menge an Pt abzuschätzen, die für die katalytische Aktivität in einem Reaktor zur Verfügung steht. Die Bindungsenergien können mit Hilfe der TPD-Methode quantifiziert werden, wie später noch erläutert wird.

Die temperaturprogrammierte Reduktion ist ein Verfahren, bei dem ein reduzierendes Gasgemisch, z. B. Wasserstoff, verdünnt in einem Inertgas, über eine Oxidprobe strömt. Die Anfangstemperatur liegt in der Regel unter der Reduktionstemperatur. Anschließend wird die Probentemperatur mit einer konstanten Rate erhöht, und mit Beginn der Reduktion wird Wasserstoff aus dem Trägergemisch verbraucht, was mit einem TCD nachgewiesen wird. Wenn die Reduktion aufhört, wird kein Wasserstoff mehr verbraucht, und die Wärmeleitfähigkeit des Gases aus dem Probenröhrchen kehrt zur Basislinie zurück. Im Verlauf des Temperaturanstiegs können mehrere Reduktionsspitzen festgestellt werden, da die Reduktion wahrscheinlich bei verschiedenen thermischen Energieniveaus eingeleitet wird. Jeder Peak entspricht dann einem anderen Oxid, und die Amplitude jedes Peaks ist proportional zur Reaktionsgeschwindigkeit.
Eisenoxid in Form von Hämatit weist drei Phasen der Reduktion auf, die den drei Eisenoxiden entsprechen. Eine TPR-Analyse von Hämatit wurde mit einem Reduktionsgas, bestehend aus 10 % Wasserstoff in Argon, und einer Temperaturrampe von 10 °C/min durchgeführt. Abbildung 6 zeigt die Ergebnisse. Der erste Reduktionspeak erscheint bei 575 K, was dem Übergang von Fe2O3 zu Fe3O4 entspricht. Der Peak bei 627 K entspricht der Umwandlung von Fe3O4 in FeO. Der letzte Peak bei 748 K entspricht dem Übergang von FeO zu Fe. Die Positionen der in Abbildung 6 gezeigten Maxima können je nach Teilchengröße des Fe2O3und anderen Parametern wie der Temperaturanstiegsgeschwindigkeit von Probe zu Probe etwas abweichen.
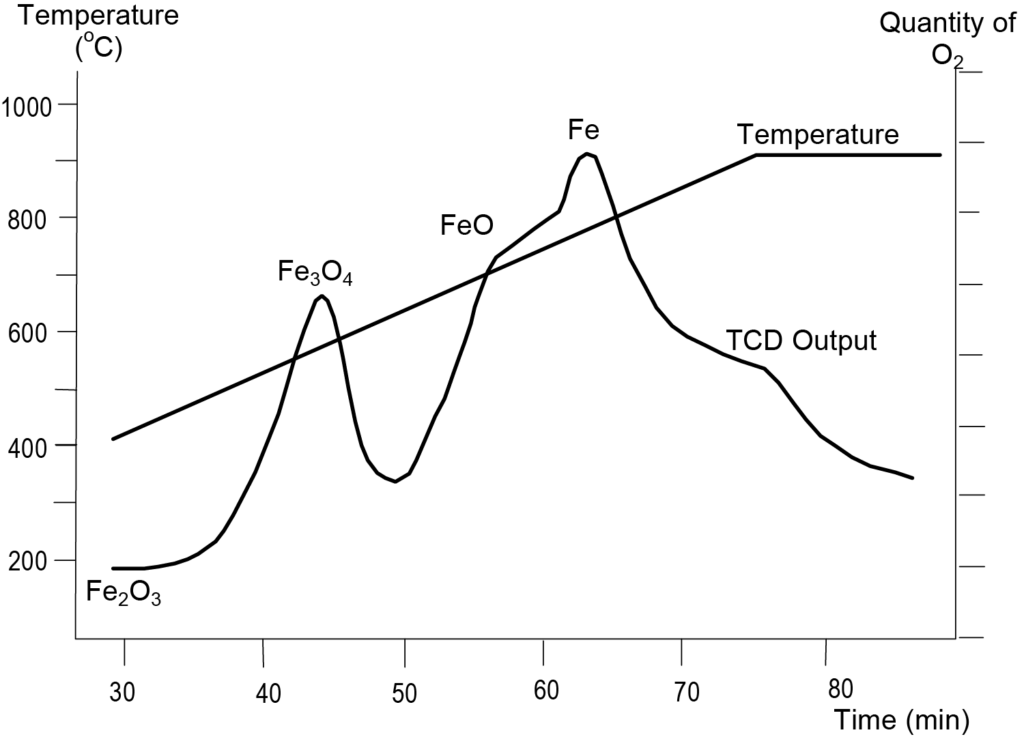
Die temperaturprogrammierte Oxidation kann zur Bestimmung der Menge der reduzierten Spezies (auch Reduktionsgrad genannt) verwendet werden, aber die Schwierigkeit bei dieser Art von Analyse besteht darin, eine vollständige Oxidation zu erreichen. Häufiger wird die TPO für Anwendungen wie die Untersuchung der Verkokungskinetik, die Bewertung des Kohlenstoffabbrandes des Katalysators, die Bestimmung der verschiedenen Formen von kohlenstoffhaltigen Ablagerungen auf den Katalysatoren nach einer CO-Zersetzungsreaktion oder, allgemeiner ausgedrückt, für Messungen des Sauerstoffverbrauchs und der Produktausbeute verwendet.
Die Probe wird mit gleichmäßiger Geschwindigkeit erhitzt, während das Reaktionsgas, in der Regel 2 % bis 5 % Sauerstoff, der Probe in Pulsen oder alternativ in einem kontinuierlichen Strom zugeführt wird. Die Oxidationsreaktion findet bei einer bestimmten Temperatur statt und führt zu einer Sauerstoffaufnahme. Die Menge des während der Reaktion verbrauchten Sauerstoffs hängt mit der Menge einer Spezies auf der Oberfläche zusammen.
Oberflächenenergie und Kinetik erster Ordnung
Die Adsorptions- und Desorptionsmechanismen setzen sich aus einer Kombination elementarer kinetischer Schritte zusammen. So kann beispielsweise ein zweiatomiges Molekül adsorbiert werden, oder es kann bei der Annäherung an die Oberfläche in Atome zerfallen, die unabhängig voneinander adsorbiert werden. Der erste Fall wird als nicht-dissoziative Chemisorption oder Kinetik erster Ordnung bezeichnet, der zweite Fall als dissoziative Chemisorption oder Kinetik zweiter Ordnung. Die Kinetik erster Ordnung wird in den folgenden Diskussionen im Vordergrund stehen.
Die Wechselwirkung eines einzelnen, isolierten Moleküls mit einer Oberfläche kann in einem Diagramm der potenziellen Energie in Abhängigkeit vom Abstand von der Oberfläche dargestellt werden, wie in Abbildung 7. Zum Vergleich enthält Abbildung 7 auch ein Energiediagramm für die Physisorption sowie den Nettoenergiepfad, den das chemisorbierte Molekül nimmt. Bei der Betrachtung dieses Diagramms ist zu beachten, dass es sich um eine grundlegende Darstellung eines einzelnen Moleküls handelt, das sich einer Oberfläche nähert, und dass nur die Energie als Funktion des Abstands von der Oberfläche betrachtet wird, während andere Variablen vernachlässigt werden.
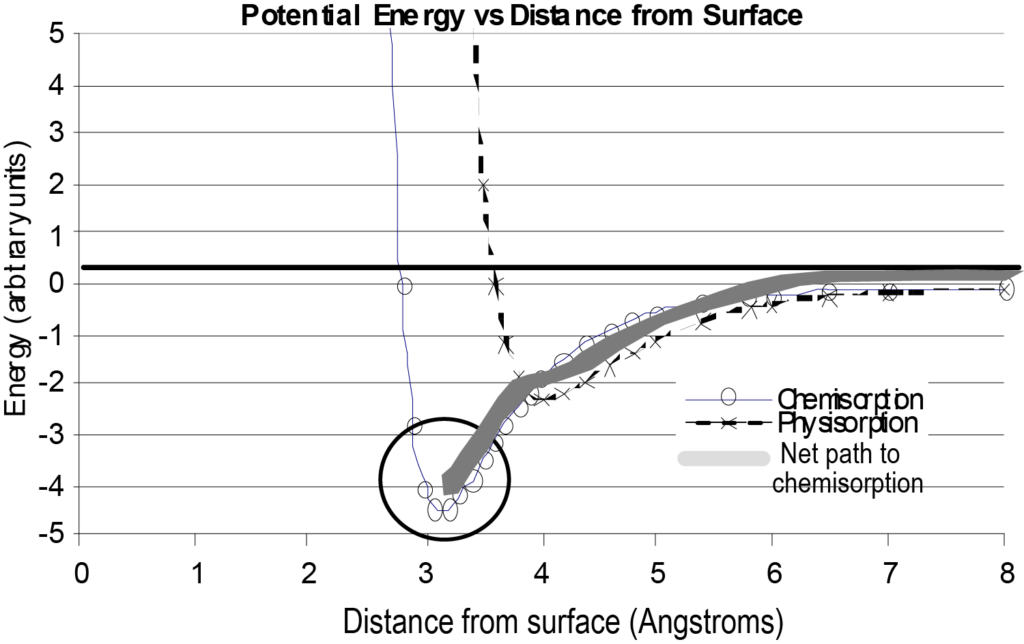
Eine Situation, die die Form der Chemisorptionskurve in Abbildung 7 stark verändern würde, wäre, wenn der Adsorptionsprozess dissoziativ wäre. Dissoziative Chemisorption erfordert einen Energieaufwand (Dissoziationsenergie), um das adsorptive Molekül zu spalten. Dies würde dazu führen, dass der Netto-Energiepfad einen positiven Peak kurz vor der negativ verlaufenden potenziellen Energiequelle aufweist. Dies ist in Abbildung 8 dargestellt. Wie in Abbildung 8 ist der physikalische Adsorptionspfad zunächst günstiger (niedrigere Energie), wenn sich das Molekül der Oberfläche nähert, aber um zu dissoziieren und chemisorbieren, ist ein positiver Energieschritt erforderlich, um den Übergang zum Chemisorptionspfad zu schaffen. Diese Energie ist größer als die dissipierte potenzielle Energie des Moleküls.
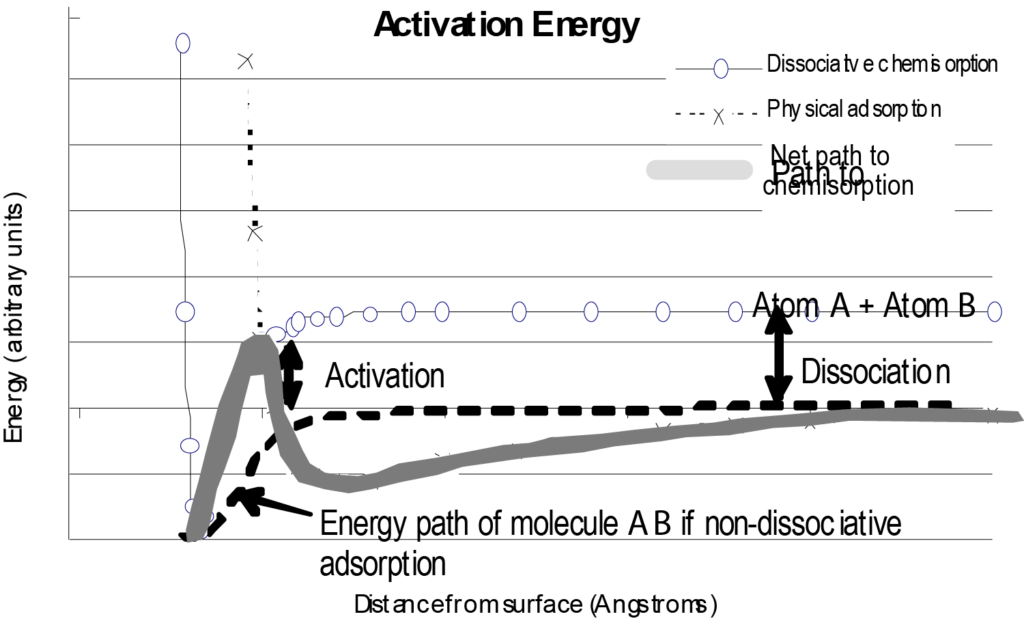
Eine wichtige Variable, die die Form der nicht-dissoziativen Chemisorptionsenergiekurve verändert, ist die Anzahl der bereits an der Oberfläche adsorbierten Moleküle. Die energiereichsten Stellen (die tiefsten Potentialtöpfe) werden zuerst besetzt. Dieser Prozess setzt sich fort, bis schließlich die Stellen mit der niedrigsten Energie besetzt sind. Die aufgetragene Energie als Funktion der Oberflächenbedeckung (Beladung) charakterisiert den Grad der Heterogenität der Oberflächenenergie. Diese Darstellung liefert wertvolle Informationen über die Katalysatoraktivität unter bestimmten Bedingungen. Für einige Anwendungen kann anstelle einer Darstellung der Oberflächenenergieverteilung ein einziger Wert für die mit der Reaktion verbundene Energie ausreichen.
Bei der Adsorption handelt es sich um einen exothermen Prozess, bei dem letztlich Energie(Adsorptionsenergie) freigesetzt wird, auch wenn ein gewisser Energieaufwand(Aktivierungsenergie) erforderlich ist, um den Prozess in Gang zu setzen. Die Umkehrung der Adsorption erfordert einen Energieaufwand, wobei die erforderliche Größe die Tiefe des Potenzialtopfs ist.
Die Abbildungen 7 und 8 beziehen sich auf die potenzielle Energie eines einzelnen, isolierten Moleküls, aber es ist das Energiepotenzial aller Teilchen im System, das bestimmt, ob sich das System im Gleichgewicht befindet. Im Gleichgewicht sollte ein Molekül an jeder Stelle des Systems das gleiche Energiepotenzial aufweisen; dies gilt für Moleküle in der Gas- oder Dampfmasse, die den Festkörper umgibt, und für die adsorbierten Moleküle an der Festkörperoberfläche.
Für ein bestimmtes Adsorbat-Adsorptionsmittel-System wird das Adsorptionsgleichgewicht durch ein empfindliches Gleichgewicht zwischen dem Druck P der Hauptgasphase, der analytischen Temperatur T und dem Grad der Oberflächenbedeckung ϑ erreicht . Experimentell wird einer dieser Parameter konstant gehalten, dem anderen wird ein Wert zugewiesen, und der dritte wird beobachtet, um seinen Wert im Gleichgewicht zu bestimmen. Eine Isotherme gibt den Grad der Oberflächenbedeckung als Funktion des Drucks bei konstanter Temperatur an (ϑ = f(P)T), eine Adsorptionsisobare drückt den Grad der Oberflächenbedeckung als Funktion der Temperatur bei konstantem Druck aus (ϑ = f(T)P), und eine Isosterie zeigt die Beziehung zwischen Druck und Temperatur für einen konstanten Bedeckungsgrad. (P = f(T)ϑ).
Die Clausius-Clapeyron-Gleichung drückt die Adsorptionswärme bei einem bestimmten Oberflächenbedeckungsgrad ϑ in Form von Druck und Temperatur aus und liefert somit die isosterische Adsorptionswärme qst. Die Gleichung in partieller Differentialform lautet
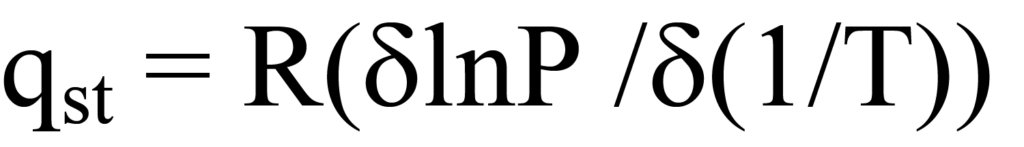
wobei T die Temperatur, P der Druck und R die Gaskonstante ist.
Um für einen bestimmten Bedeckungsgrad zusammenhängende Temperatur- und Druckwerte zu erhalten, werden mehrere Isothermen derselben Probe bei unterschiedlichen Temperaturen ermittelt und die Achse der adsorbierten Menge in Einheiten von Bedeckungsgraden skaliert. Auf diese Weise lässt sich aus den Isothermen eine Reihe von Isobaren extrahieren, die über den in den Analysen verwendeten Temperaturbereich als Bedeckungsgrad gegen die Temperatur aufgetragen werden. Aus der Reihe der Isobaren kann eine Reihe von Druck-/Temperaturwerten für verschiedene Werte des adsorbierten Volumens extrahiert werden. Diese werden als ln(P) vs. 1/T aufgetragen.
Die obige Clausius-Clapeyron-Gleichung kann in die lineare Form y = m(x) umgruppiert werden und ergibt
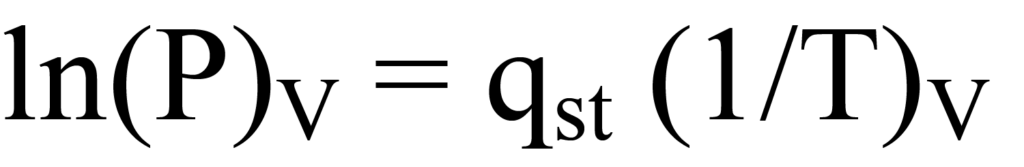
R ist eine Skalierungskonstante, die keinen Einfluss auf die Steigung hat. Für jeden Wert der adsorbierten Menge gibt es eine andere Steigung, qst. Wenn man die Steigungen in Abhängigkeit von der adsorbierten Menge aufträgt, erhält man das gesuchte Diagramm der Oberflächenenergie im Verhältnis zur adsorbierten Menge, das sich auf die Oberflächenbedeckung oder -beladung bezieht.
Die Adsorptionswärme kann auch anhand von Daten berechnet werden, die mit der dynamischen Chemisorptionsmethode gewonnen wurden, die manchmal als "Heizratenvariation" bezeichnet wird. Da die adsorbierte Menge als Funktion des Drucks bei der dynamischen Methode nicht überwacht wird, muss ein anderer Energieausdruck als in den Gleichungen 10 und 11 gesucht werden. Zu Übungszwecken wird ein solcher Ausdruck in den folgenden Abschnitten abgeleitet. Das Ergebnis (Gleichung 21) kann im Vertrauen auf die Richtigkeit übernommen und verwendet werden, ohne dass man sich mühsam durch die Mathematik wühlen muss. Die schrittweise Ableitung wird hier jedoch vorgestellt, weil sie für einige Leser von Interesse sein könnte und eine detaillierte Ableitung in der Literatur nur schwer zu finden ist. Teile des folgenden Textes wurden aus Arbeiten von Schroeder und Gottfried, Houston, Nix und Garrett entnommen.
Die Desorption beinhaltet die zeitliche Änderungsrate der Anzahl der adsorbierten Moleküle N, algebraisch ausgedrückt als ΔN/Δt. Dies kann auch als die zeitliche Änderungsrate der Anzahl der verfügbaren Adsorptionsstellen Na angesehen werden.
(Anmerkung: Zeit- und temperaturabhängige Änderungen werden mathematisch bequemer behandelt, indem man jeden Zeit- oder Temperatursprung als infinitesimal klein betrachtet. Dadurch kann DN/Dt durch ΔN/Δt ersetzt werden und die algebraische Manipulation wird durch die Differentialrechnung ersetzt. Für Leser, die mit der Infinitesimalrechnung nicht vertraut sind, kann jeder Ausdruck der Form dX/dY als die Steigung einer Kurve von X gegen Y bei einem bestimmten Wert von X betrachtet werden).
Der kinetische Ausdruck für die Desorptionsrate Rd lautet
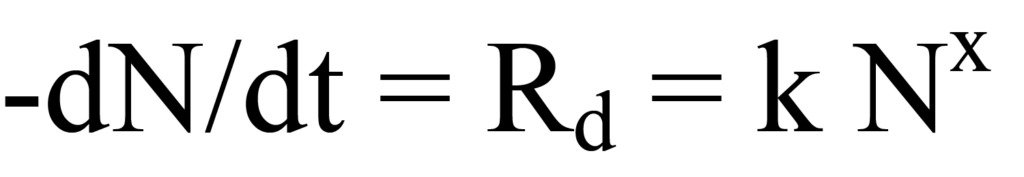
wobei k die Geschwindigkeitskonstante, -N die momentane Oberflächenkonzentration (Anzahl) der adsorbierten Spezies (negativ bedeutet abnehmend) und x die kinetische Ordnung ist. Nur der einfachste Fall, die Kinetik erster Ordnung (nicht dissoziativ), wird hier betrachtet; daher ist x=1. Man beachte, dass sich die Desorptionsrate ständig ändert, wenn die Anzahl der auf der Oberfläche verbleibenden Moleküle abnimmt.
Die Abbildungen 8 und 9 veranschaulichen, dass eine Aktivierungsenergie erforderlich sein kann oder auch nicht, um die Adsorption in Gang zu setzen. Diese Abbildungen verdeutlichen jedoch auch, dass es immer eine Aktivierungsbarriere gibt, die überwunden werden muss, damit das Molekül desorbiert wird, d. h. die Chemisorptionsoberflächenreaktion sich umkehrt. Die Beziehung zwischen der Geschwindigkeitskonstante und der Energie bei energieabhängigen Reaktionen wie der Desorption kann in einer Arrhenius-Form ausgedrückt werden, nämlich
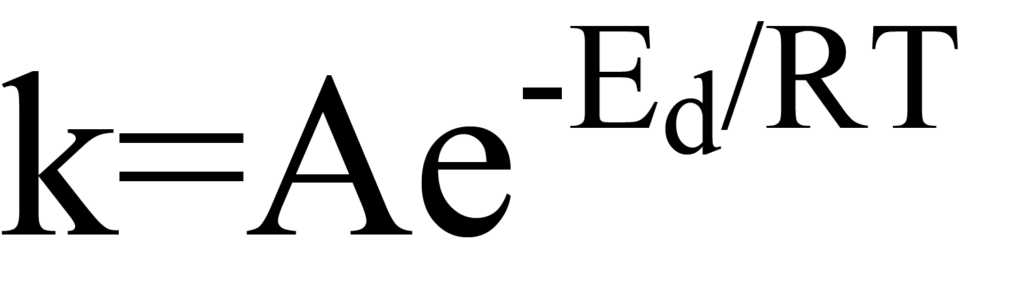
wobeiEdes die Aktivierungsenergie ist und der Index "d" den speziellen Fall der Desorption kennzeichnet. Der vorexponentielle Faktor A kann als die Anzahl der Versuche des Moleküls pro Zeiteinheit angesehen werden, aus dem Potentialtopf zu entkommen. T ist die Temperatur (Grad Kelvin) und R die universelle Gaskonstante. Das Produkt RT ist die thermische Energie, der Exponent E/RT ist also das Verhältnis von Aktivierungsenergie zu thermischer Energie. Solange E größer als RT ist, ist die Wahrscheinlichkeit der Desorption gering.
Setzt man den Arrhenius-Ausdruck in Gl. 8 ein, erhält man
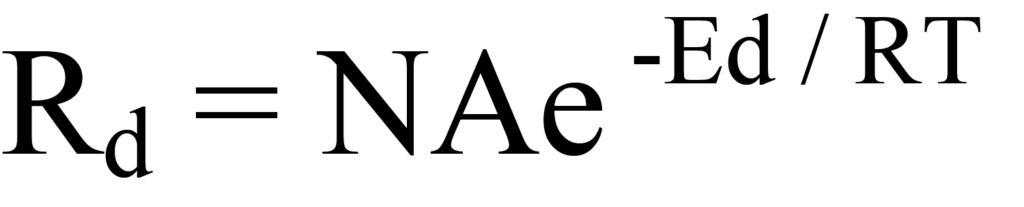
Dies ist die Polanyi-Wigner-Gleichung für die Desorptionsrate erster Ordnung. Man kann mit dieser Gleichung experimentieren, um besser zu verstehen, was sie in Bezug auf die Desorption beschreibt. Die Änderung der Desorptionsrate (Rd), des Bedeckungsgrads (N) und des Energieverhältnisses (Ed/RT) in Abhängigkeit von der Temperatur sind in Abbildung 10 dargestellt, wobei die Werte der Einfachheit halber auf der vertikalen Achse normiert sind. Bei einem tatsächlichen Experiment würde die Detektorleistung der Desorptionsrate entsprechen. Die Temperatur Tm, bei der die Desorptionsrate am höchsten ist, ist in Abbildung 10 leicht zu erkennen, da sie in einem Diagramm des Detektorsignals (Menge der entstandenen Molekülspezies) gegen die Temperatur aufgetragen ist.
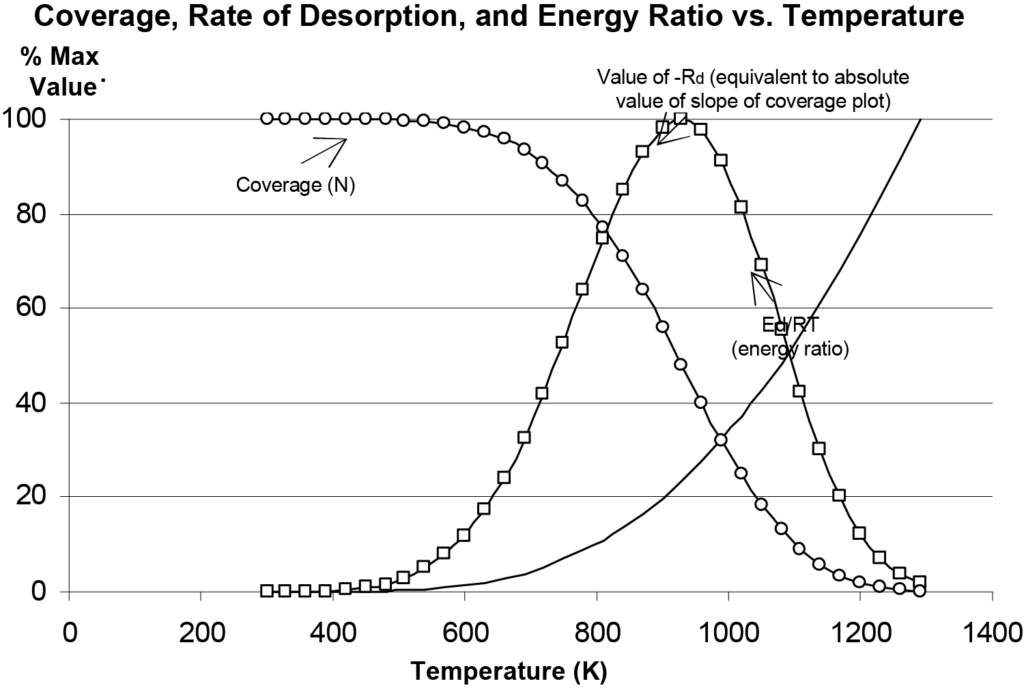
Hinweis: Abbildung 10 wurde von Microsoft Excel® unter Verwendung von Gl. 14 und beliebigen Werten für die Parameter erstellt. Dies ermöglicht das Experimentieren mit den Parametern und den Vergleich verschiedener Diagramme, die durch das Polanyi-Wigner-Modell vorhergesagt werden. Es ist zu beobachten, dass die Spitzen etwas asymmetrisch um Tm herum verlaufen. Eine Erhöhung des anfänglichen Bedeckungswertes bewirkt, dass die Amplitude der Spitze zunimmt, wobei Tm konstant bleibt. Eine Erhöhung des Wertes von A bewirkt, dass sich der Peak zu niedrigeren Temperaturen hin bewegt. Eine Erhöhung von Ed bewirkt, dass der Peak breiter wird und der Maximalwert bei höheren Temperaturen auftritt.
Die Extraktion des Logarithmus beider Seiten von Gleichung 10 ergibt
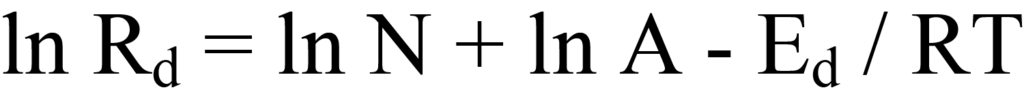
Die Umformung dieser Gleichung in eine lineare Form, y = (m)x +(b), ergibt
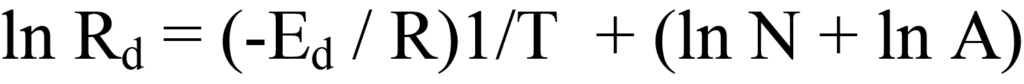
Trägt man ln Rd gegen 1/T auf, ergibt sich eine Gerade mit der Steigung -Ed/R und dem Achsenabschnitt (ln N + ln A). Das Problem ist hier, dass keine Zahlenwerte für Rd verfügbar sind, so dass die Ableitung erweitert werden muss.
Bei einem temperaturprogrammierten Analysetest wird die Probe linear erhitzt, so dass die Temperatur T zu jedem Zeitpunkt t wie folgt berechnet werden kann
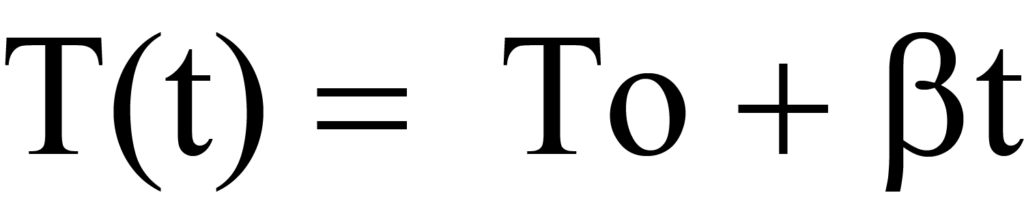
oder
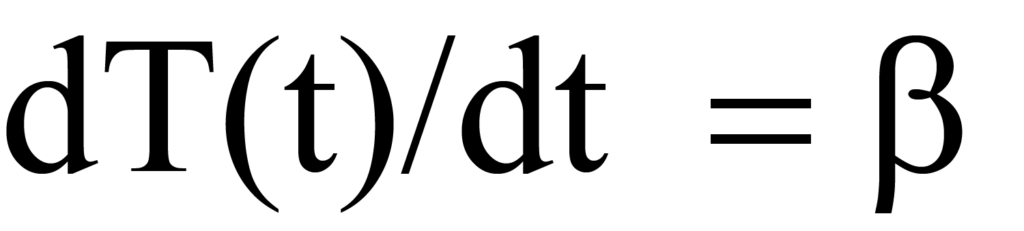
wobei β die Heizrate oder Rampenrate dT/dt in Grad K pro Zeiteinheit ist. Mit steigender Temperatur ändert sich die Anzahl der pro Zeiteinheit desorbierten Moleküle, ausgedrückt durch dN/dT. Multipliziert man die zeitabhängige Heizrate (dT/dt) in Grad/min mit der temperaturabhängigen Desorptionsrate (-dN/dT) in Molekülen/Grad, erhält man die zeitabhängige Desorptionsrate Rd. Mathematisch gesehen,
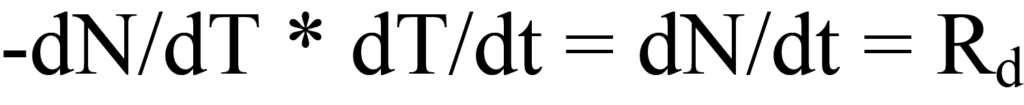
Die Erwärmungsrate β wurde in Gl. 15a als dT/dt definiert, daher ergibt die Substitution in die linke Seite von Gl. 12
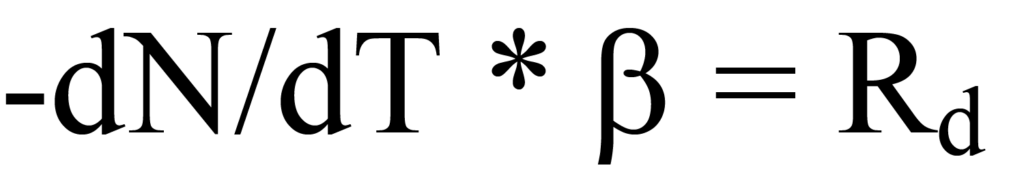
Durch Einsetzen von Gl. 17 in Gl. 14 ergibt sich
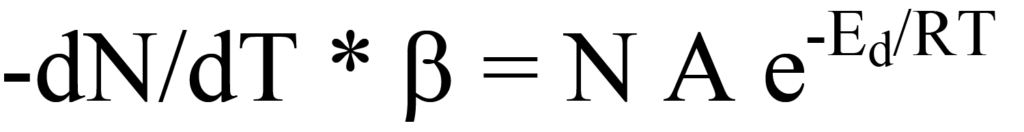
und Umlagerung ergibt die temperaturabhängige Desorptionsrate,
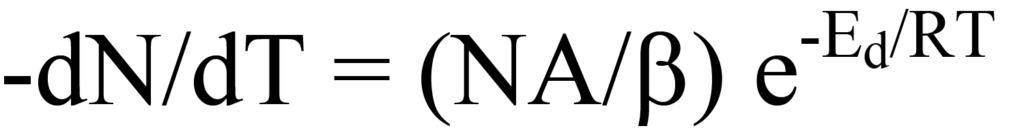
die das Diagramm der Desorptionsrate in Abbildung 10 beschreibt. Mit steigender Temperatur erreicht die Desorptionsrate bei Tm ihr Maximum, und bei dieser Temperatur ist die Steigung (erste Ableitung) von Gl. 15 gleich Null, d. h.,
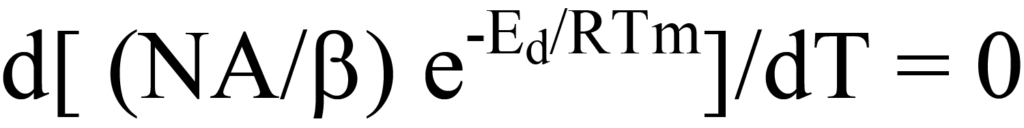
Der Klarheit und Kontinuität halber wird der Leser daran erinnert, dass Gleichung 20 die Form d(uv)/dT hat, wobei u = (A/b)N, v = e-Ed/RT und N eine Funktion der Temperatur (T) ist.
Gleichung 20 ergibt
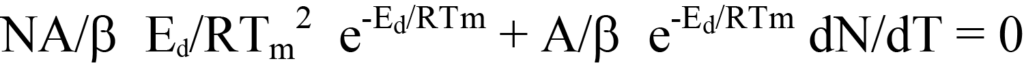
Setzen Sie nun die rechte Seite von Gleichung 19 für dN/dT (ein negativer Wert; siehe Gleichung 12) in Gleichung 13 ein und faktorisieren Sie. Dies ergibt
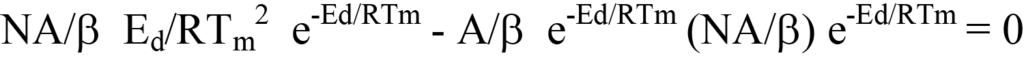
oder
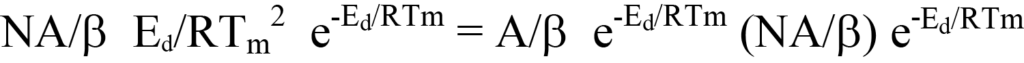
Eliminiert man die gemeinsamen Begriffe auf der linken und rechten Seite, so bleibt Folgendes übrig
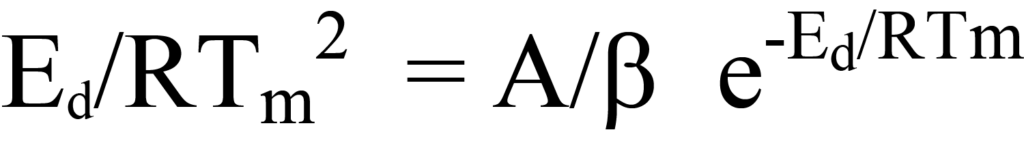
Die Werte von Tm, β und R sind bekannt; A ist unbekannt, ebenso wieEd, der gesuchte Wert. Ein Ansatz zur Bestimmung der Unbekannten besteht darin, die Terme der Gleichung 23 in linearer Form auszudrücken, y = mx + b. Dies kann durch Umformung erfolgen zu
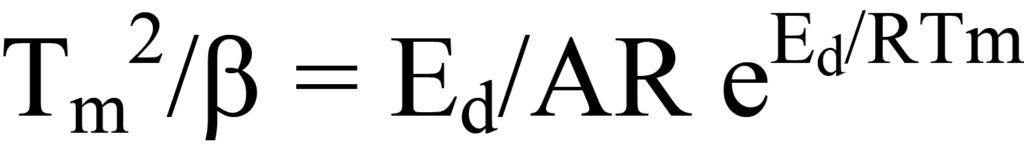
Wenn man den Logarithmus jeder Seite nimmt, erhält man

eine lineare Gleichung, in der y = ln Tm 2/β, x = 1/Tm, m =Ed/R und b = lnEd/AR. Das Auftragen von y gegen x für eine Reihe von β-Werten ermöglicht die Bestimmung vonEd. Eine andere Form der Gleichung 25a, die manchmal in der Literatur zu finden ist, ergibt sich aus der Erweiterung der logarithmischen Terme, um
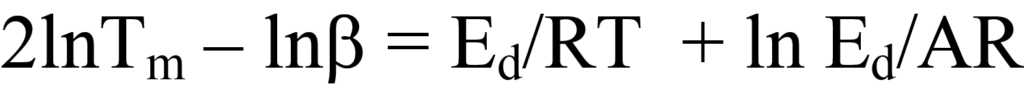
Eine andere Möglichkeit, von Gleichung 22a zu Gleichung 25 zu gelangen, besteht darin, die letztgenannte Gleichung zu faktorisieren und umzustellen.
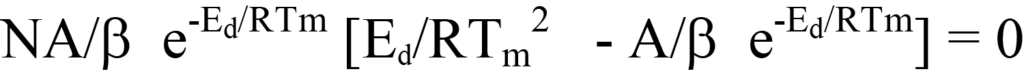
Dividiert man beide Seiten dieser Gleichung durch den Ausdruck in den Klammern, erhält man
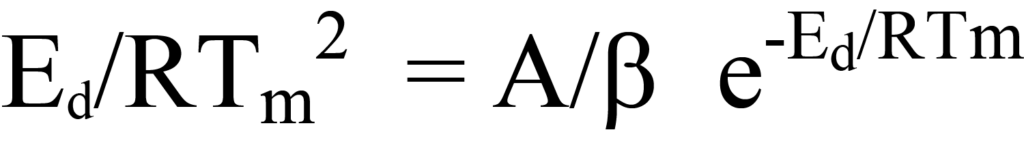
was mit Gleichung 23 übereinstimmt.
Es gibt auch den Fall
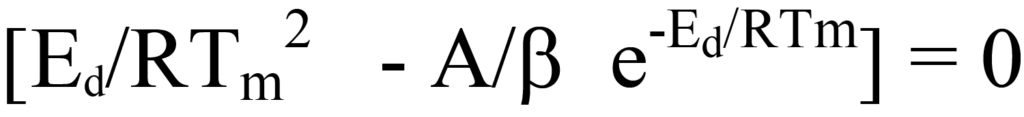
oder
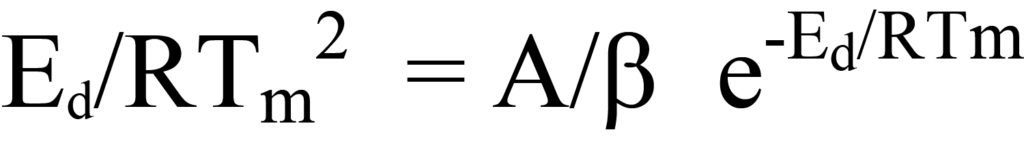
durch Division beider Seiten von Gleichung 26 durch die Faktoren außerhalb der Klammern oder durch logische Ableitung, dass der Ausdruck in den Klammern von Gleichung 26 gleich Null sein muss, da weder der Faktor NA/β noch e-Ed/RT während des Desorptionsprozesses einen Wert von Null hat. Durch Umstellen erhält man
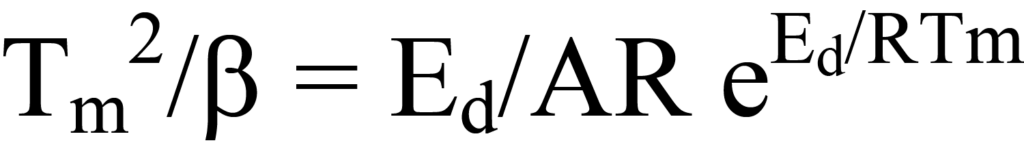
was mit Gleichung 24 übereinstimmt.
Nach der Methode von Redhead wird die Gleichung 25 wie folgt umgestellt:
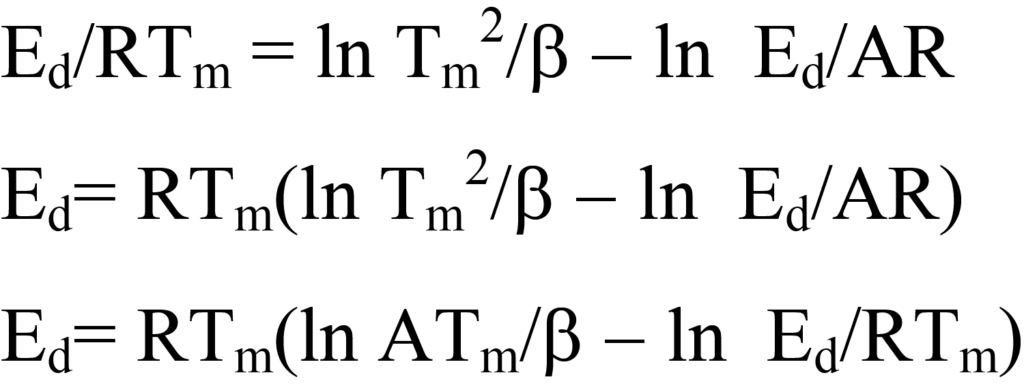
Diese Gleichung wird vereinfacht, indem der Term ln Ed/RTm auf der rechten Seite auf 3,64 geschätzt wird, was einen Fehler von weniger als 1,5 % für Werte von A/β zwischen108/K und 1013/K einführt, wobei A für die Kinetik erster Ordnung typischerweise auf 1013/s angenähert wird. Somit,
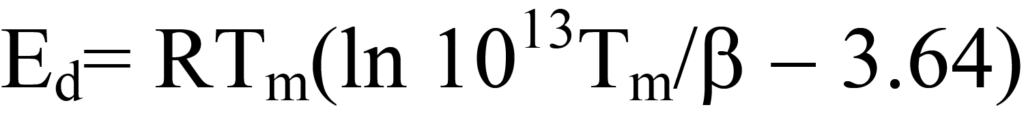
Ähnlich wie bei der Einpunktmethode zur Bestimmung der BET-Oberfläche ist diese Methode mit einem gewissen Fehler behaftet, aber sie ermöglicht es,Ed aus einem einzigen Desorptionschromatogramm zu schätzen. (Schroeder und Gottfried). Anstatt den Wert von A zu schätzen, könnte man eine Reihe von Chromatogrammen für verschiedene β-Werte erstellen und die Werte vonEd und A aus der linearen Darstellung bestimmen.
Bei der Anwendung der Redhead-Methode ist zu bedenken, dass sie nur für die Kinetik erster Ordnung gilt. Im Hinblick auf Reaktionen höherer Ordnung mahnt Stoltz (Stoltze): "E, das auf diese Weise erhalten wird, als Näherung zu bezeichnen, ist eine Untertreibung, völlig falsch wäre eine bessere Beschreibung."
Zusammenfassung
Feste Katalysatoren spielen eine Rolle "hinter den Kulissen", indem sie viele Vorteile des täglichen Lebens erschwinglich und sogar möglich machen. Die Chemisorption ist ein grundlegender Schritt bei katalytischen Reaktionen, so dass es von großem Nutzen ist, den Chemisorptionsprozess im kleinen Maßstab im Labor zu untersuchen. Moderne Analyseinstrumente, mit denen diese Reaktionen charakterisiert werden können, sind leistungsstarke Werkzeuge für die Überwachung und Kontrolle der Herstellung und Anwendung von Katalysatoren und für die Vorhersage der Leistungsmerkmale neu entwickelter Katalysatormaterialien.
Ressourcen
James P. Olivier, Thermodynamic Properties of Confined Fluids I: Experimental Measurements of Krypton Adsorbed by Mesoporous Silica From 80K to 130K, The 2nd Pacific Basin Conference on Adsorption Science and Technology, University of Queensland, Brisbane, Australien, Mai 2000.
Sven L.M. Schroeder und Michael Gottfried, Temperaturprogrammierte Desorption (TPD) und Thermische Desorptionsspektroskopie (TDS), Freie Universität, Berlin (Internet http://userpage.chemie.fuberlin. de/~pcfp/V18/pdf/v18.pdf).
Paul L. Houston, Cornell University Chemical Kinematics and Reaction Dynamic, Ithaca.
Roger Nix, An Introduction to Surface Chemistry, Fachbereich Chemie, Queen Mary University of London (World Wide Web http:// www.chem.qmw.ac.uk/surfaces/scc/scat2_4.htm).
Simon J. Garrett, Einführung in die Oberflächenchemie (Vorlesungsunterlagen), Michigan State University.
W.J. Moore, Physikalische Chemie, Prentice-Hall, Inc. (1972).
J.H. de Boer, The Dynamical Character of Adsorption, Oxford at the Clarendon Press (1953).
G.C. Bond, Heterogeneous Catalysis- Principles and Applications, Claredon Press, Oxford (1987).
John H. Sinfelt, Structure of Metal Catalysts, Review of Modern Physics, Vol. 51, No. 3 (1979).
Thomas H. Maugh, Industry Steps Up Quest for Catalysts, High Technology, August 1984.
Scholten, Pijpers und Hustings, Surface Characterization of Supported and Nonsupported Hydrogenation Catalysts, Catal. Rev.-Sci. Eng., Vol. 27, No. 1, (1985).
A. Baiker, Experimentelle Methoden zur Charakterisierung von Katalysatoren. II. X-Ray Diffraction, Temperature- Programmed Desorption and Reduction, Thermogravimetry and Differential Thermoanalysis, International Chemical Engineering, Vol. 25, No. 1 (1985).
Philip Moriarty, Atoms and Molecules at Surfaces, School of Physics & Astronomy, University of Nottingham ( World Wide Web http:// www.nottingham.ac.uk/~ppzpjm/sect4_2.htm).
M. B. Raschke, U. Ho, Chemisorption energy of hydrogen on silicon surfaces, Physical Review B, Volume 63.
P. A. Redhead, The Ultimate Vacuum, Vakuum 12, 203-211, 1962.
Per Stoltze, Introduction to heterogeneous catalysis- Concepts and calculations, Department of Physics, Technical University of Denmark.
Gerard P. van der Laan, Kinetics, Selectivity and Scale Up of the Fischer-Tropsch Synthesis, Dissertation, Universität Groningen, Niederlande, 1999.