Introducción
La adsorción por ruptura ofrece muchas ventajas sobre las mediciones de adsorción estática. Las mediciones de penetración de multicomponentes se realizan haciendo fluir múltiples corrientes de gas o vapor. Un espectrómetro de masas mide la concentración de salida de la columna de ruptura. A continuación, los datos se evalúan para determinar el rendimiento de adsorción y separación de un material. Las mediciones de multicomponentes pueden analizarse utilizando un espectrómetro de masas para una gran variedad de gases y vapores. Para los compuestos isoméricos, que tienen espectros de masas que se solapan, el FTIR es el instrumento preferido para analizar la concentración de salida de un sistema de ruptura.
En esta nota, se analizan mezclas de vapor de uno y varios componentes en busca de zeolita 13X en elBreakThrough Analyzer (BTA) Micromeritics . Se analizaron independientemente flujos de vapor de agua y etanol, masas 18 y 46 respectivamente, utilizando un espectrómetro de masas. Estas mediciones se realizaron a 50 °C utilizando flujos equimolares de gas portador de nitrógeno y helio.
El sistema de avance genera corrientes de vapor haciendo fluir un gas inerte a través de un borboteador. Los burbujeadores han demostrado ser muy eficaces en la generación de corrientes de vapor saturado a bajos caudales. Todos los componentes del sistema de avance se alojan dentro de una caja caliente, lo que evita la condensación de las corrientes de vapor y permite mantener una temperatura constante durante todo el análisis. El agua y el etanol a 50 °C en un gas portador inerte generarán una corriente saturada a las siguientes presiones de vapor: agua 0,124 bar y etanol 0,292 bar.
Experimental
Se realizaron tres experimentos de adsorción de vapor en la zeolita 13X utilizando agua, etanol y una mezcla de agua y etanol. Se utilizaron nitrógeno y helio como gas portador y gas trazador para las mediciones de adsorción, ya que ambos son inertes. Antes del análisis, la muestra se activó a 100 °C durante una hora y a 200 °C durante otras 12 horas bajo flujo de gas nitrógeno para eliminar cualquier especie adsorbida.
En primer lugar, se realizó un análisis de vapor de agua al 50% de HR utilizando una corriente dividida de nitrógeno seco y helio humidificado. El experimento se realizó a una presión de 1,0 bar y una temperatura de 50 °C. Para este experimento se utilizó un caudal total de 24 sccm, 12 sccm eran de helio humidificado y 12 sccm de nitrógeno seco. La presión de vapor del agua a esta concentración es de 0,124 bar.
A continuación, se volvió a analizar el vapor de etanol utilizando una corriente dividida de nitrógeno seco y helio humidificado. El experimento se realizó a una presión de 1,0 bar y una temperatura de 50 °C. Se utilizó un caudal total de 24 sccm compuesto por 12 sccm de helio saturado de etanol y 12 sccm de nitrógeno seco. La presión de vapor del etanol a esta concentración es de 0,292 bar.
Se realizó un experimento final utilizando corrientes mezcladas de etanol y vapor de agua. El experimento se realizó a una presión de 1,0 bar y una temperatura de 50 °C. Se utilizó un caudal total de 24 sccm compuesto por 12 sccm de nitrógeno saturado de agua y 12 sccm de helio saturado de etanol. Las presiones de vapor del agua y del etanol son las mismas que las indicadas anteriormente.
Resultados
Agua
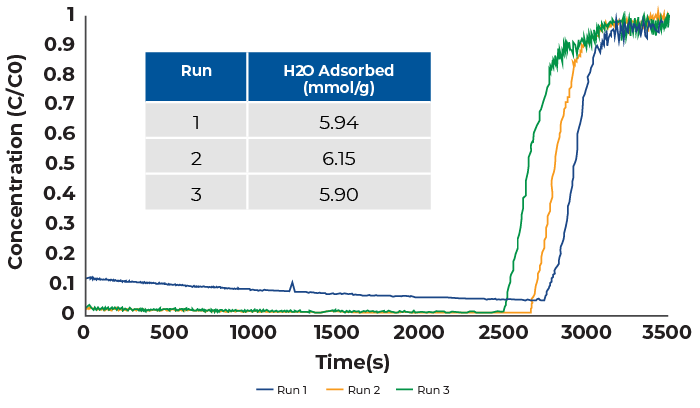
Las mediciones de la penetración de vapor de agua se realizaron mezclando un flujo de nitrógeno seco con un flujo de helio saturado de agua en una proporción de uno a uno. El caudal total fue de 24 sccm, compuesto por 12 sccm de nitrógeno y 12 sccm de helio. Los resultados se muestran en la Figura 1.
La curva de penetración del agua muestra que la zeolita 13X adsorbe una cantidad considerable de agua aunque la concentración sea baja (la presión de vapor es de 0,124 bar). La penetración se produjo aproximadamente a los 45 minutos del experimento en todas las mediciones, y las curvas de penetración resultantes fueron nítidas, de modo que las limitaciones de transferencia de masa son mínimas. Entre cada experimento, la muestra de zeolita 13X se reactivó durante la noche a 200 °C. Este paso es necesario ya que el agua se adsorbe en la muestra. Este paso es necesario ya que el agua se adsorbe fuertemente en la zeolita 13X y fue necesario para una reactivación completa. Además, el agua es difícil de eliminar de los espectrómetros de masas, por lo que antes de cada medición el espectrómetro de masas se horneó durante varias horas para expulsar el agua de la atmósfera fuera del sistema.
Etanol
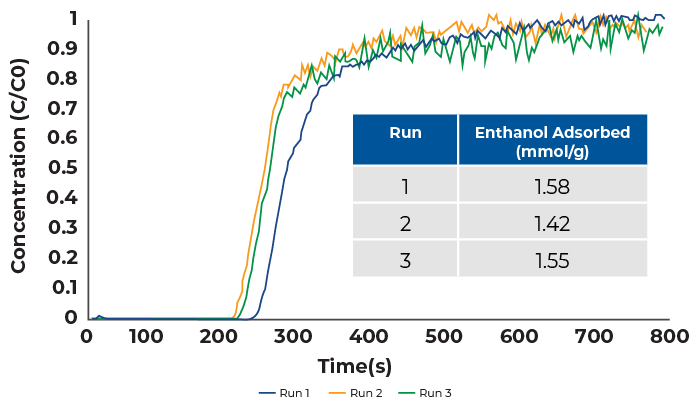
Los experimentos de penetración de vapor de etanol se realizaron mezclando una corriente de nitrógeno seco con una corriente de helio saturada de etanol en una proporción de uno a uno. El caudal total fue de 24 sccm, compuesto por 12 sccm de nitrógeno y 12 sccm de helio. Los resultados se muestran en la Figura 2.
Las mediciones posteriores de la penetración de etanol se realizaron primero sin reactivación térmica durante la noche. Se hizo pasar una corriente pura de nitrógeno a través de la columna durante dos horas, pero se produjo una caída sustancial de la capacidad de adsorción de etanol. La capacidad en el segundo paso descendió a 0,49 mmol/g. Para las pruebas aquí mostradas, la zeolita 13X fue reactivada durante la noche a 200 °C para todas las mediciones.
Las curvas de penetración del etanol muestran que hay una caída mínima en la capacidad de adsorción entre series. Durante el primer ciclo, se adsorbieron 1,58 mmol/g de etanol, frente a 1,42 mmol/g en el segundo ciclo y 1,55 mmol/g en el tercero. Todas las curvas de ruptura son pronunciadas, lo que significa que las limitaciones de transferencia de masa no fueron un problema durante estos análisis.
Etanol-agua
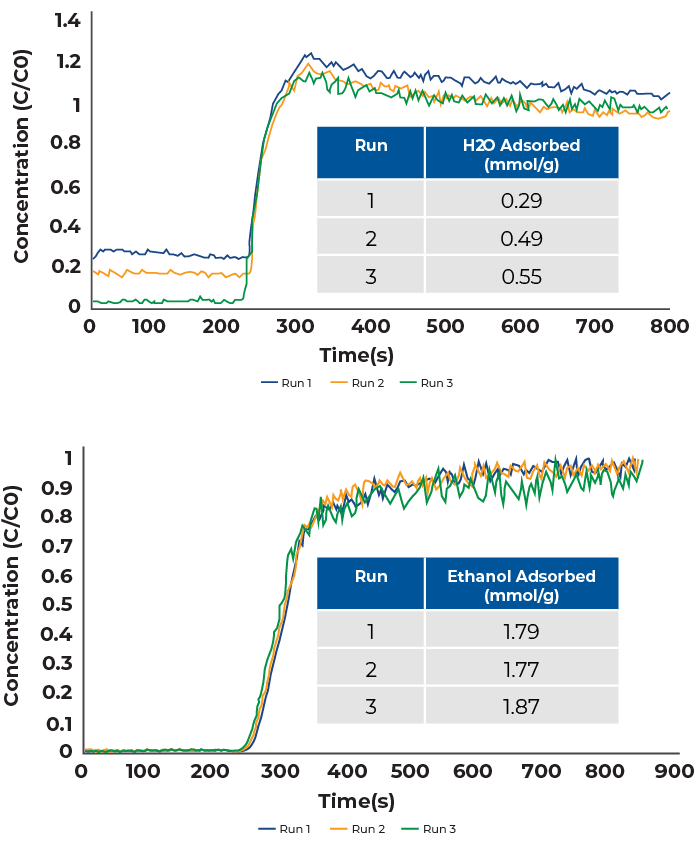
Los experimentos de ruptura etanol-agua se realizaron mezclando una corriente de helio saturada de agua con una corriente de nitrógeno saturada de etanol. El caudal total fue de 24 sccm, compuesto por 12 sccm de nitrógeno y 12 sccm de helio. Mientras que los caudales de nitrógeno y helio eran iguales, los caudales de etanol y agua diferían, ya que el agua tiene una presión de vapor inferior a la del etanol a 50 °C. Los resultados de la ruptura se muestran en la figura 3.
Entre cada medición, las muestras se reactivaron durante la noche a 200 °C para eliminar todo el etanol y el agua adsorbidos. Antes de las mediciones de adsorción, también se horneó el espectrómetro de masas para eliminar el agua y el etanol que quedaban en él.
Las curvas de penetración del agua y el etanol muestran un comportamiento típico de adsorción competitiva. Además, el agua y el etanol son parcialmente miscibles, por lo que es probable que se produzca un efecto sinérgico en su comportamiento de adsorción. El vapor de agua penetra ligeramente antes que el etanol y muestra un ligero enrollamiento antes de alcanzar la saturación. Las curvas de rotura del etanol son similares a las de la figura 2, aunque la capacidad de adsorción ha aumentado ligeramente. Como ya se ha mencionado, es probable que esto se deba a un efecto sinérgico de la adsorción combinada de agua y etanol. La capacidad de adsorción de vapor de agua se ha suprimido significativamente en comparación con las mediciones anteriores y disminuye aún más debido a la adsorción preferencial de etanol. La adsorción preferente de etanol se debe en parte a su mayor concentración por tener una mayor presión de vapor a 50 °C.
Conclusiones
La nota de aplicación mostró la adsorción de componentes puros de agua y etanol en la zeolita 13X, así como la adsorción competitiva de estas dos especies. La tabla 1 resume las capacidades de adsorción de las tres mediciones. En el experimento de ruptura multicomponente agua-etanol, se observó una adsorción preferencial de etanol. En todas las mediciones no se observó ninguna caída de presión. Además, las curvas de penetración eran pronunciadas, de modo que las limitaciones de transferencia de masa eran insignificantes.
